キャンバスのニュース
キャンバス、免疫着火剤「CBP501」の欧州第3相試験開始へ申請・準備を継続 後続パイプラインにも動きあり
会社概要

加登住眞氏(以下、加登住):本日はお集まりいただき、ありがとうございます。取締役CFOの加登住です。ただいまより、株式会社キャンバス2026年6月期第2四半期決算説明会を開催します。
まず、会社概要についてです。これまでと同様ですので詳細は省略しますが、従業員数はわずかに増加しており、研究開発部門などの採用が進んでいます。
キャンバスの企業価値の源泉

キャンバスの企業価値の源泉のご説明です。1つ目は有望な最先⾏化合物「CBP501」です。臨床第2相試験まで有望な臨床データを伴って終了しており、現在は臨床第3相試験の申請を進めています。また、こちらは自前の創薬パイプライン型の開発で進めています。
2つ目は、「CBT005」や「CBS9106」など、後続のパイプラインを持ち継続的に新薬候補を創出する体制を整えていることです。
「CBP501」の臨床開発の進捗が企業価値に大きな影響を与えると考えられがちですが、もちろんそれも1つの要素である一方で、企業価値の源泉となっているのはこの2点であることを、改めてご説明しておきたいと思います。
キャンバスの強み がん免疫に着目したパイプライン戦略
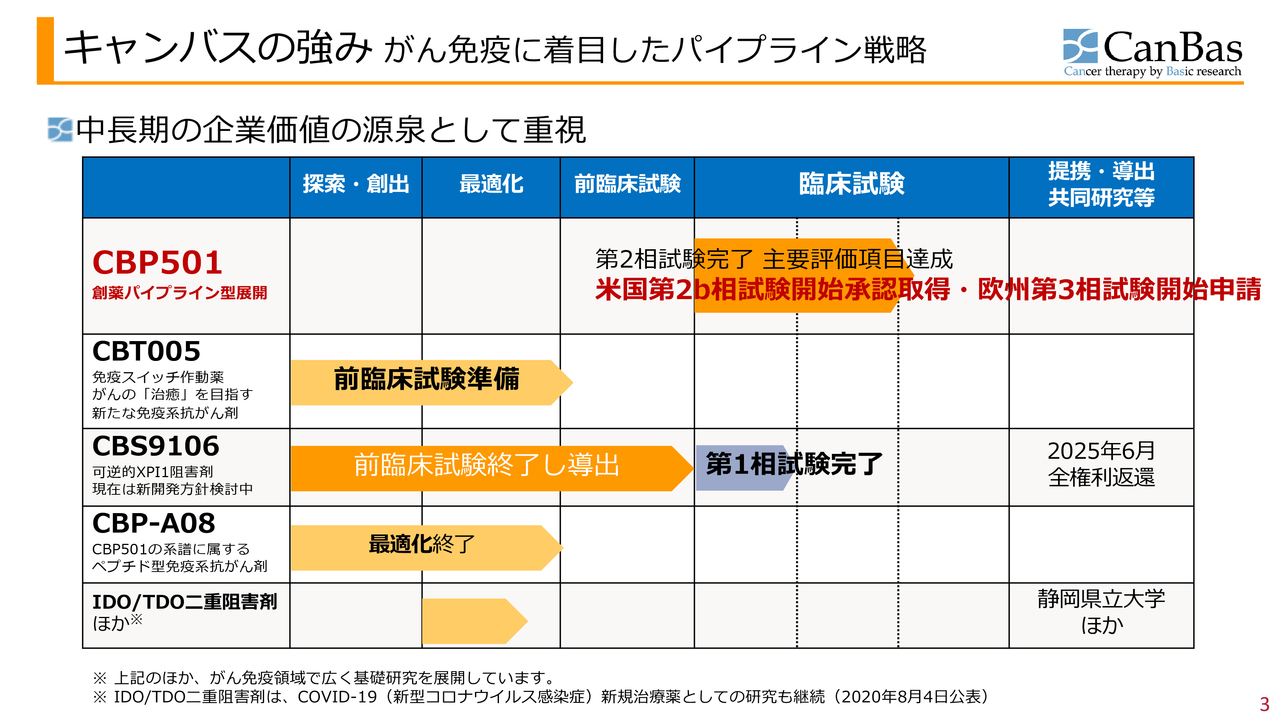
河邊拓己氏(以下、河邊):代表取締役社長の河邊です。現在、キャンバスが保有するパイプラインはスライドのとおりです。最重要パイプラインである「CBP501」と、その次に「CBT005」が続きます。さらに「CBS9106」「CBP-A08」、その他が控えています。
各パイプラインの歩み・現状・目標

各パイプラインの時間軸についてはスライドのとおりです。
免疫系抗がん剤は一部の患者様に劇的に効く
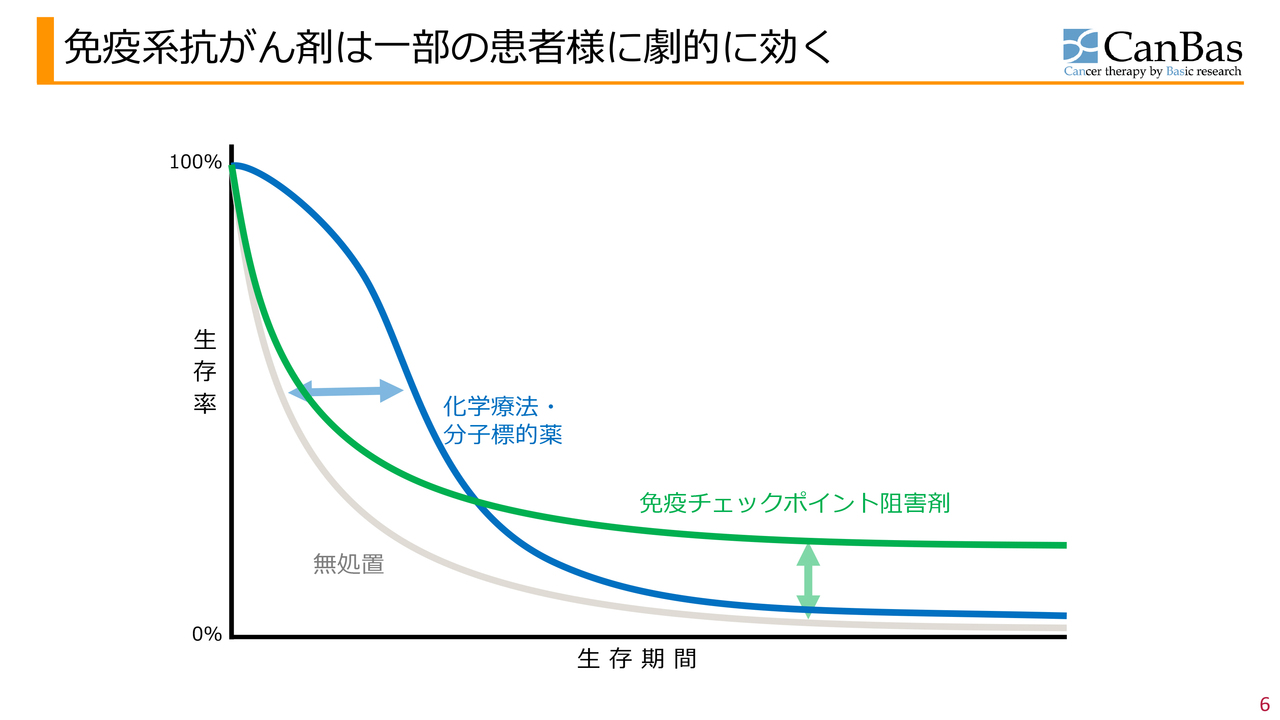
免疫着火剤と呼んでいる「CBP501」についてご説明します。スライドは、がん患者さまの生存期間を示すカプランマイヤー曲線です。横軸が生存期間、縦軸が生存率を示しており、最初に100パーセント生存している患者さまが少しずつ亡くなっていくというカーブを表しています。
青いカーブで示す化学療法(従来型抗がん剤)や分子標的薬は、多くの患者さまに効果がありますが、長期にわたっては効きにくい傾向があります。
一方で免疫チェックポイント阻害剤は、効く患者さまは少ないものの、効果があった患者さまには非常に長期にわたり効果が続く特徴があります。現在はこの免疫チェックポイント阻害型の抗がん剤の開発が主流となっています。
免疫系抗がん剤の効きにくい「免疫コールド」ながん
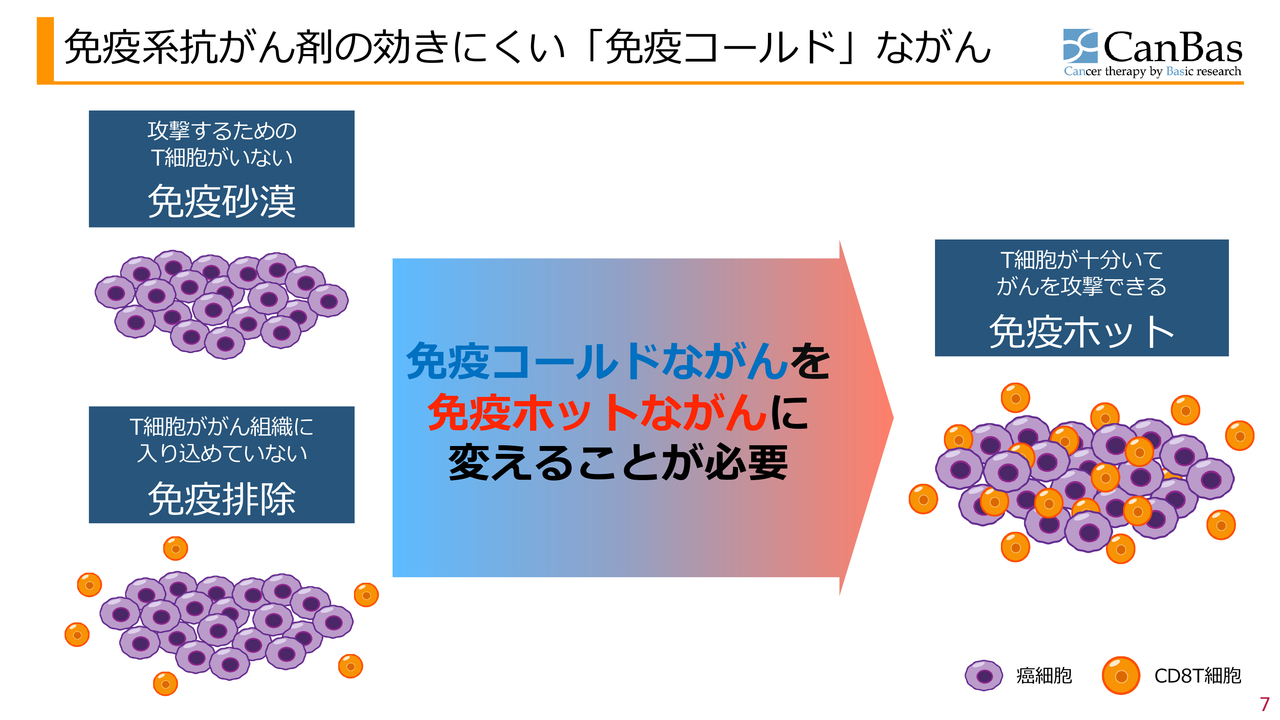
免疫系抗がん剤がどのように作用するか、あるいはなぜ作用しないのかについてのご説明です。スライドの図で示された紫色の部分はがん細胞を表しています。このがん細胞を実際に殺すうえで大きな役割を果たしているのは、オレンジ色で示したCD8T細胞です。
がんの中には「免疫砂漠」や「免疫排除」と呼ばれるタイプがあり、これらはCD8T細胞が存在しない、または存在していてもがん細胞内部に入り込まない場合があります。その代表的ながんとして膵臓がんがあります。
このようながんを、CD8T細胞ががん細胞の内部にいるような状態にすることを「免疫ホットな状態」と呼びます。このような状態にする、あるいはもともとこの状態である場合には、免疫チェックポイント阻害剤が効果を発揮しやすくなります。
CBP501の3剤併用で免疫系抗がん剤を効きやすくする
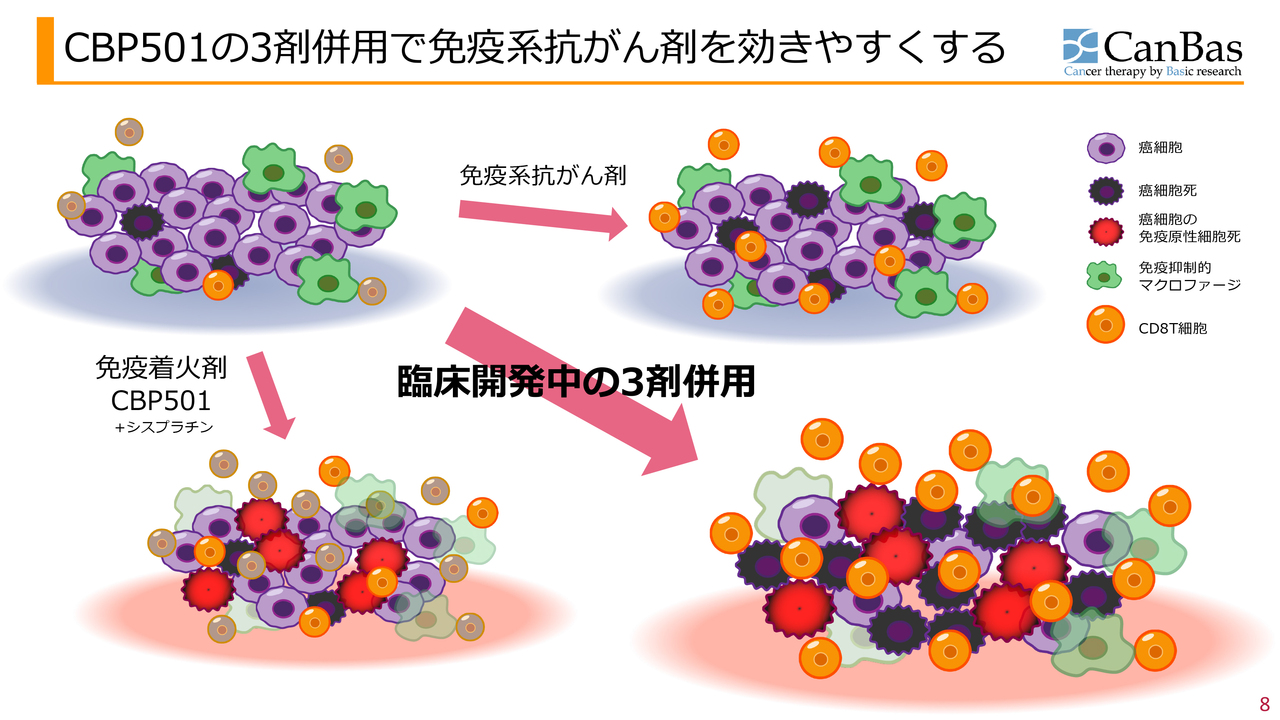
そこで、私たちの「CBP501」がどのように作用するかについてご説明します。スライドは膵臓がんをイメージしたイラストです。
スライド左上は治療を受けていない場合のイラストです。紫色のがん細胞が存在し、死んだがん細胞は黒く描かれています。オレンジ色のCD8T細胞の多くはブレーキがかかった状態の灰色で表現されています。緑色で描かれているのは免疫抑制系の細胞です。
スライド右上のイラストは免疫系抗がん剤として有名な「オプジーボ」などを投与したものです。CD8T細胞のブレーキが解除され、活性化してオレンジ色に変化します。しかしながら、免疫抑制的なマクロファージ(緑の細胞)が依然として存在しているため、CD8T細胞の数自体が少なく、効果が出にくいというのが膵臓がんの特徴です。
一方、免疫着火剤である「CBP501」と「シスプラチン」を加えたものが、スライド左下のイラストです。がん細胞が死ぬ際には、アポトーシスという、免疫を活性化しない死に方をしますが、「CBP501」は免疫を活性化する炎症が起きるような死に方に導きます。この様子を赤色とトゲトゲで表現していますが、がん細胞が派手に死ぬことで、CD8T細胞が腫瘍内部に侵入する助けとなります。
さらに、「CBP501」は免疫抑制を引き起こすマクロファージなどのサイトカイン産生を直接抑制し、それによってCD8T細胞ががん細胞の中に入ることが促進されます。
この状態で免疫チェックポイント阻害剤を使用すると、スライド右下のようにCD8T細胞が十分にがん細胞の中に入り込み、ブレーキがかかっている状態を免疫チェックポイント阻害剤が解除することで、相乗効果が期待できるということです。
CBP501臨床第2相試験データ学会発表

「CBP501」の臨床第2相試験の結果について簡単にご説明します。スライドはポスター発表された内容です。「CBP501」を投与した第1群(3剤併⽤・CBP501 25mg)と第2群(3剤併⽤・CBP501 16mg)とも良好な結果となりました。
「CBP501」「シスプラチン」「ニボルマブ」の併用療法は、転移性膵臓がんに対する3次治療として、忍容性のある安全性で、3ヶ月無増悪生存率、無増悪生存期間、全生存期間において持続的な奏効と臨床的に意義のある改善をもたらしたと発表されました。
なお、これは臨床を行った医師たちによる発表であり、当社のひとりよがりな見解ではありません。
CBP501臨床第2相試験データ論文発表
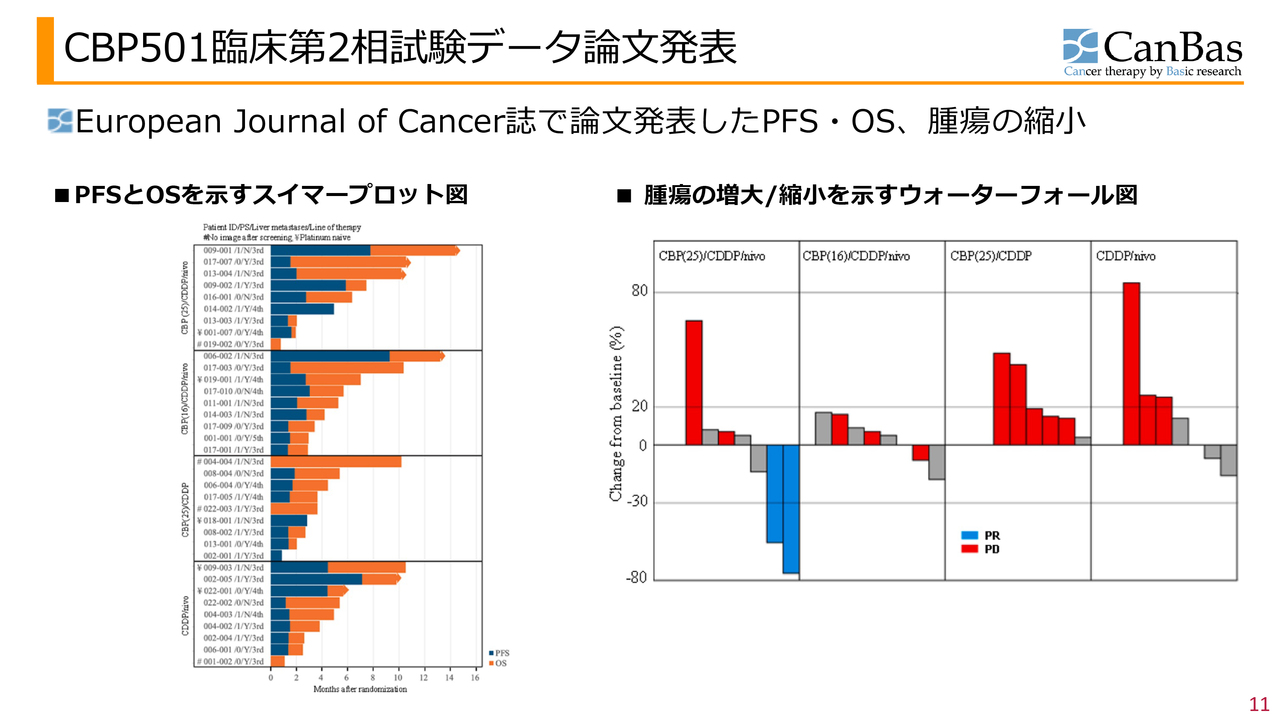
スライドは、患者の生存を示すスイマープロット図と、がんの増大・縮小を示すウォーターフォール図です。この臨床試験は4群で実施しました。そのうち当社が次の臨床試験で実施を予定しているのは第1群の組み合わせです。
最初の図の左上と右の図の最も左に示すとおり、第1群で良好な効果が出ています。
CBP501臨床第2相試験データ
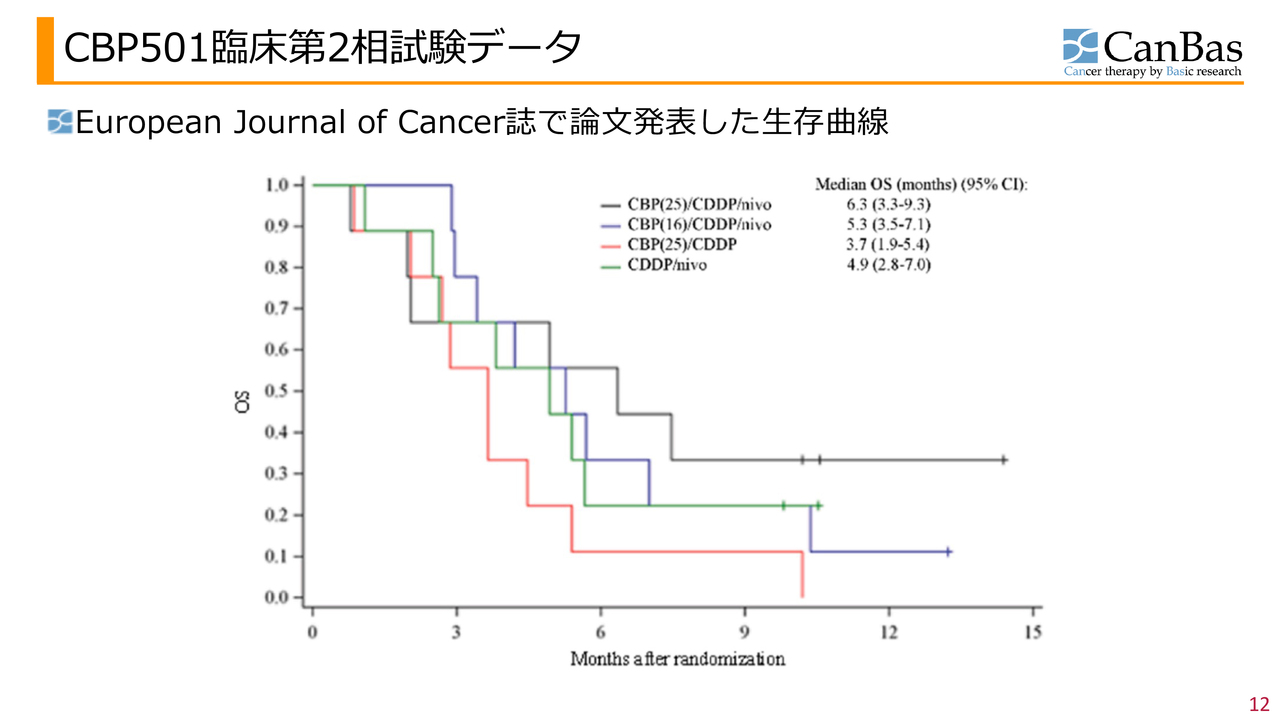
スライドはカプランマイヤー生存曲線です。凡例の一番上が「CBP501」の推奨投与量の群です。
目指してきた「最適な併用」への前進
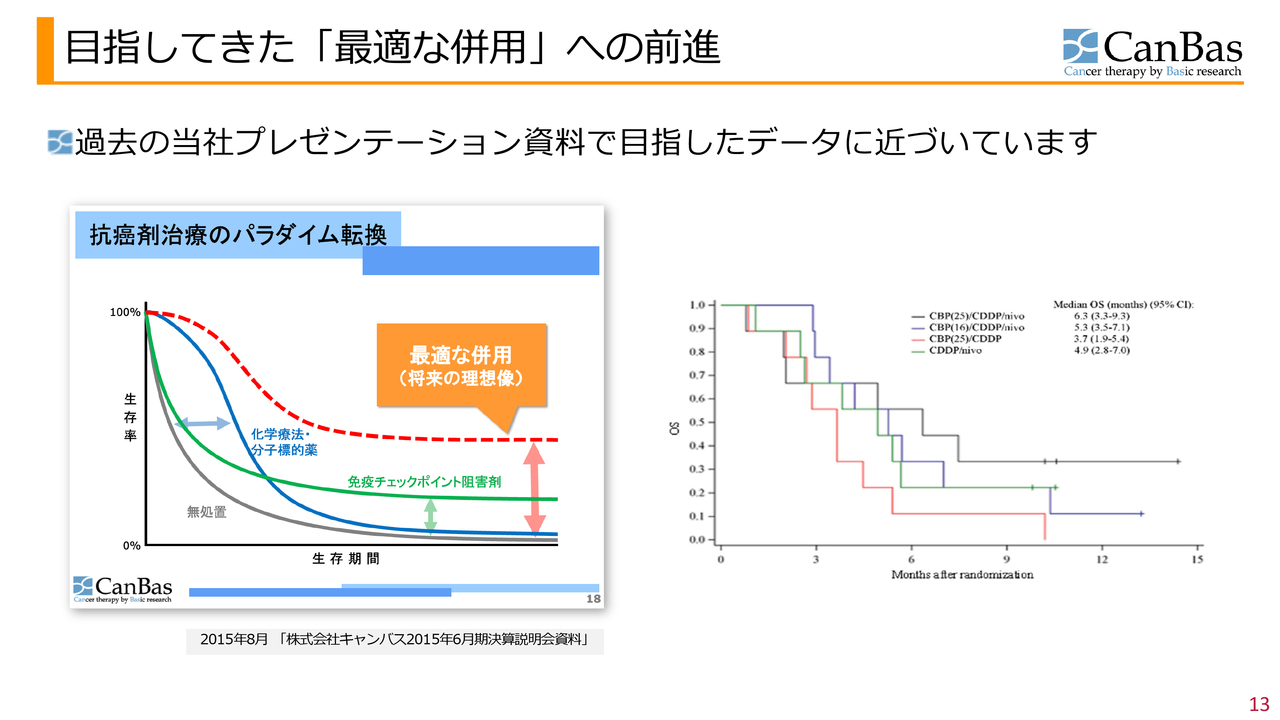
我々は2015年に、抗がん剤のパラダイム転換に関する資料として、スライド左側のカプランマイヤー曲線を提示しました。分子化学療法・分子標的薬を青で、免疫チェックポイント阻害剤を緑で示し、将来的にはオレンジ色の点線が示すカーブを目指しているとご説明しました。
今回の臨床試験の結果では、黒い線で示すとおり、そのイメージに似た傾向が見られました。
右の図の赤い線は、従来型治療法で得られると予想される生存曲線に重なります。実際にはもう少し悪い結果になるかもしれないと考えています。
このように、臨床試験の第2相試験は非常に良好な結果であったと考えています。
欧州第3相試験開始申請・準備の現状と開発目標

これを基に、現在「CBP501」は欧州での臨床試験準備を進めています。その中での「開始承認取得の不確実性」についてご説明します。
まず「時期に関する不確実性」については、当社でコントロール不能な要素が現在も存在しています。これについては当局とのやり取りが背景にあり、当社として予測が難しい部分があるため、いつどのようになるのかを確実にお伝えできる状況にはありません。
「開始承認取得の時期以外の不確実性」については、「臨床試験のデザインそのものに問題があるのではないか」「大きな意味を持たない試験になってしまうのではないか」といった点が挙げられます。この点に関しては、現時点で大きな問題は認められません。
「開始承認を受領後に試験を迅速に開始するための準備」については、欧州では国が複数存在し、今回の臨床第3相試験では多くの施設を利用する予定です。そのため、契約交渉など多くの事務作業が発生しますが、これを強力に進めています。
また、時期以外の要因で状況が悪化した場合には、⽶国第2b相試験への移⾏を検討しています。米国では、臨床第2b相試験の開始許可を取得済みであり、スタートできる初期準備も完了しています。そのため、万が一の場合にはそちらを活用する手段があります。しかしながら現状ではその兆候は見られず、欧州で第3相試験を実施できる見通しで準備を進めています。
臨床第3相試験の費⽤については、現時点では変更ありません。
開発完了目標に関しては、「2027年の新薬承認を目指す可能性がある」と公表していた内容を昨年10月に撤回しました。これは「時期以外の不確実性」が顕在化したわけではなく、あくまでも「時期の不確実性」、つまり試験実施が可能そうであることには変わりないものの時期が遅れることを反映したものです。
(注)時期の不確実性・時期以外の不確実性

「時期の不確実性」と「時期以外の不確実性」についてご説明します。
「時期の不確実性」とは、時間をかければ解決可能な問題を指します。これは、「私たちとしてはクリアできている、実際にクリアしている」と考えているものの、当局からは「クリアしていると言えない」状況にある問題を指します。したがって根本的な問題ではなく、時間をかければ許可やクリアが確実に得られるものです。
また、当局の許可が出るまでの期間に関しては「いつ」と明確に言えないことが多く、これも「時期の不確実性」に該当します。
一方「時期以外の不確実性」については、「根本的に誤っている」「試験内容がおかしい」、あるいは「そもそも試験を実施する意義がない」といった、大きな根本的な問題を指します。
CBT005の構造
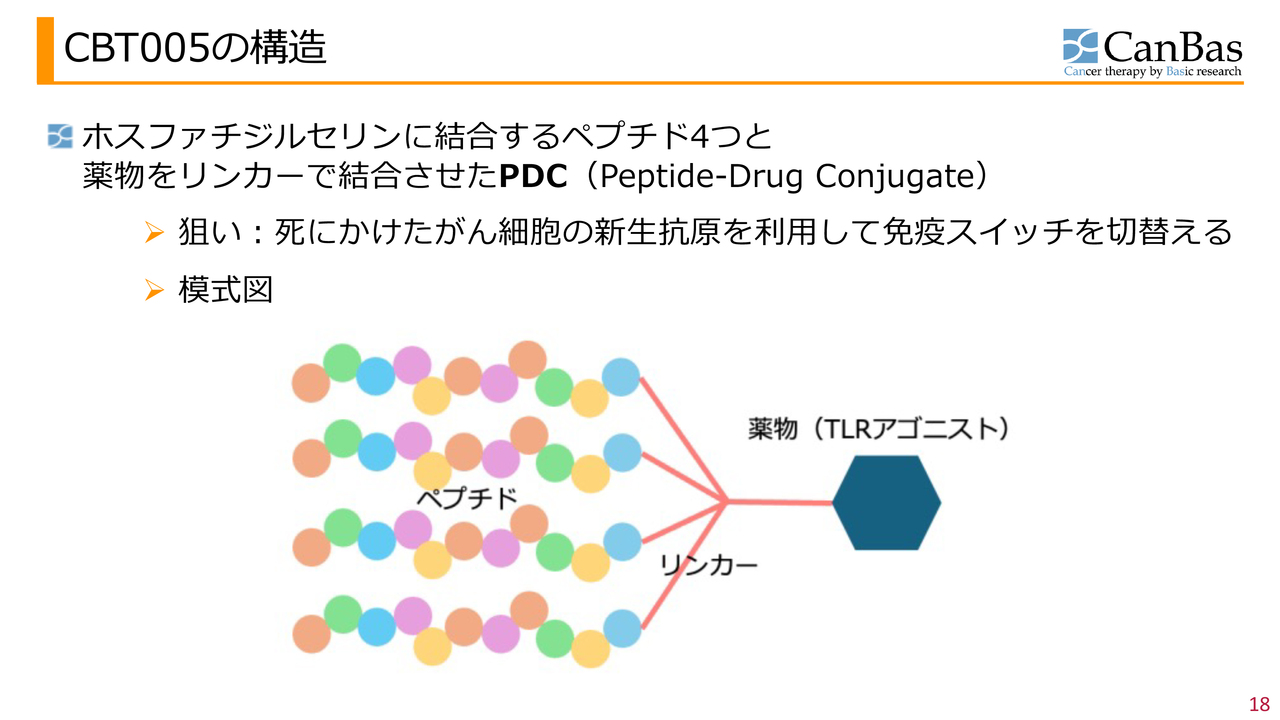
免疫スイッチ作動薬「CBT005」についてご説明します。3ページで示したパイプラインの2つ目に該当するもので、当社では非常に有望であると考えています。
現在、前臨床準備を進めています。こちらはペプチドと薬物の複合体「Peptide-Drug Conjugate」というカテゴリに属し、死にかけたがん細胞の新生抗原を利用して免疫スイッチを作動させるコンセプトのものです。
CBT005も「免疫コールド/ホット」のアプローチ
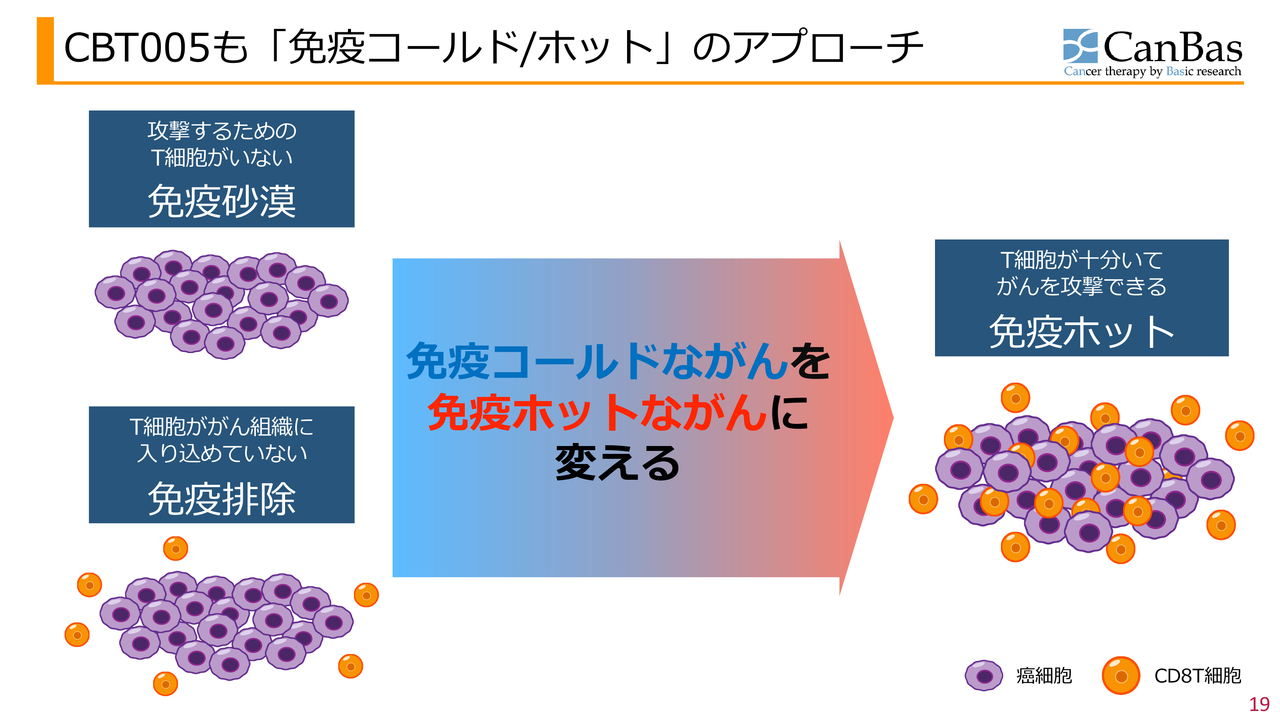
CBT005もCBP501と同様に、「免疫砂漠」「免疫排除」の状態になっているがん細胞を、免疫ホットながんに変えていきます。
CBT005の作用機序
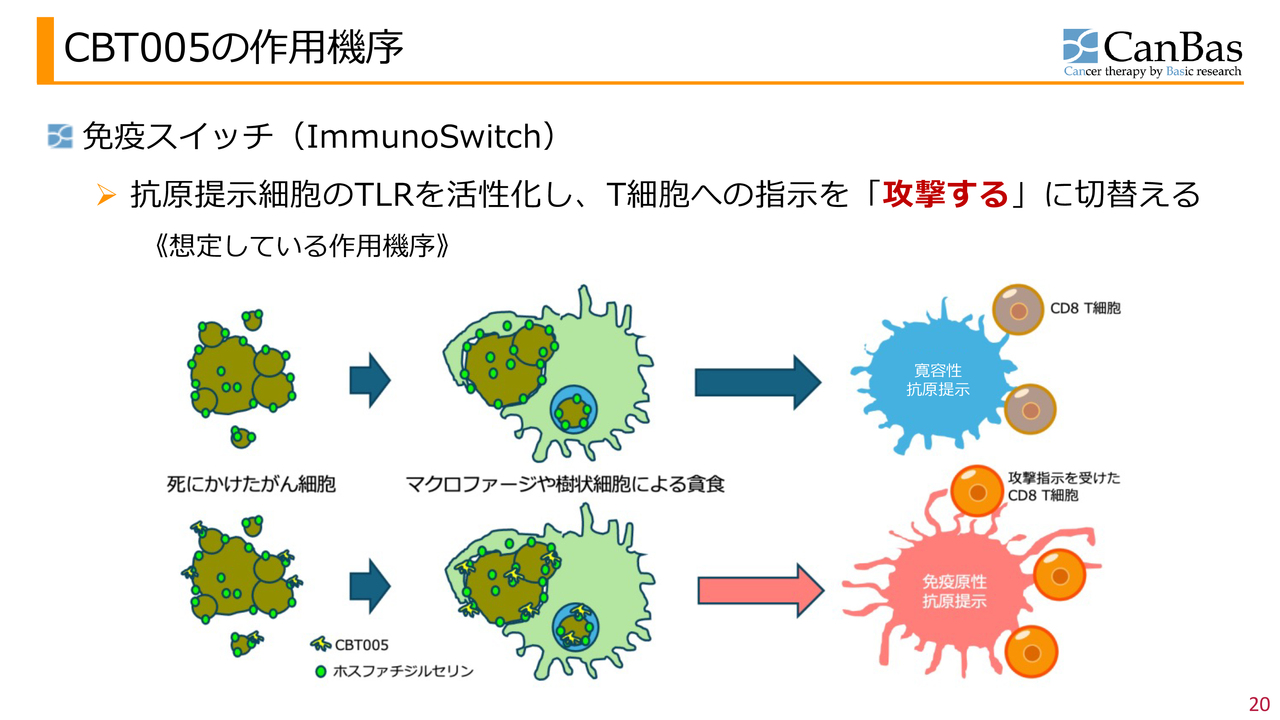
死にかけたがん細胞の表面には「ホスファチジルセリン」が数多く現れることがわかっています。その「ホスファチジルセリン」を目印に薬剤を結合させ、その薬剤を使って免疫抑制的な抗原提示を免疫活性的な抗原提示に切り替えるという狙いです。
抗原提示とは、免疫細胞ががん細胞を取り込み、がん細胞内の正常細胞とは異なる部分をCD8T細胞に伝える過程を指します。この時、「この部分は攻撃対象ではない」と伝えるのが寛容性抗原提示であり、逆に「この部分を攻撃しろ」と伝えるのが免疫原性抗原提示です。
がんを持つ患者さまの体内では、スライド上段で示された状態(寛容性抗原提示)にあることが多く、これを免疫スイッチ(ImmunoSwitch)より下段の状態に切り替えます。
こちらについては現在まだ前臨床試験に入る段階のため、もう少し時間はかかりますが、有望だと思っています。
CBT005 基礎研究から臨床開発へ

現在、前臨床試験に向けて大量合成の準備を進めていますが、他社の臨床試験でさまざまな問題点が見つかった部分を踏まえ、改良の可能性についても検討を重ねています。
基本的には「CBT005」の大量合成を予定していますが、場合によっては少し改良したものになる可能性もある状況です。
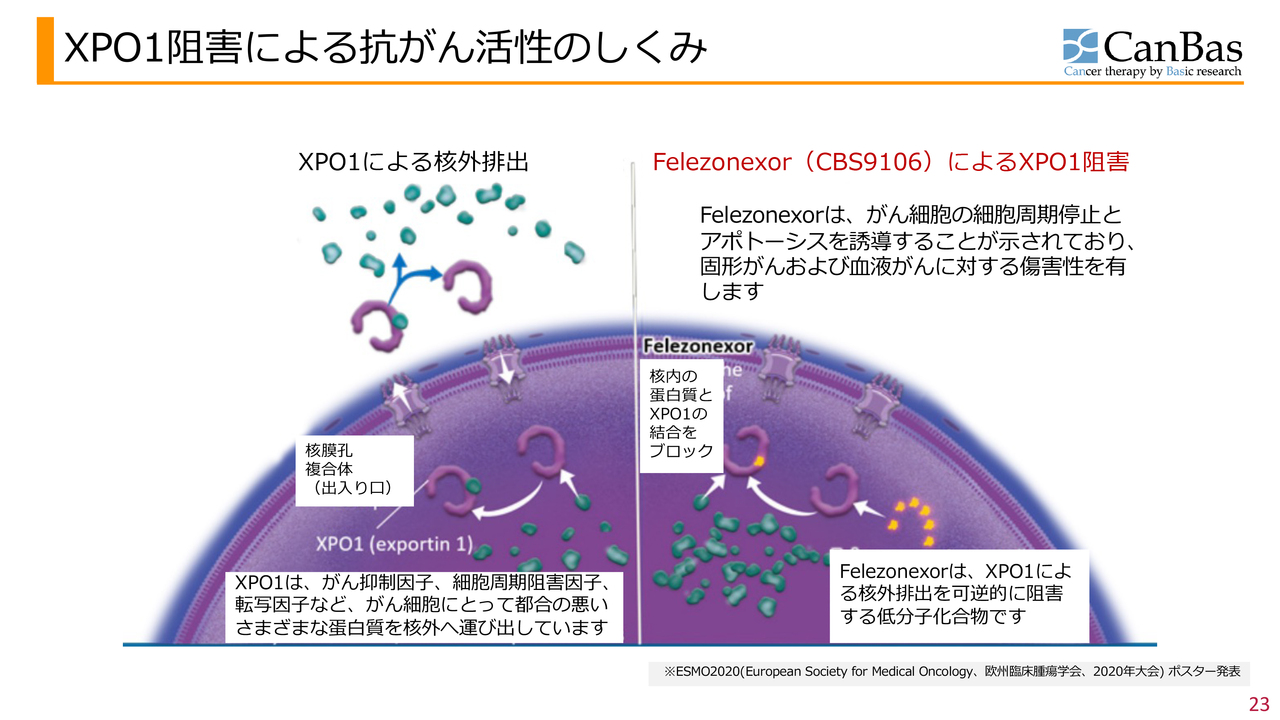
XPO1阻害による抗がん活性のしくみ
パイプラインの3つ目である可逆的XPO1阻害剤「CBS9106」についてご説明します。こちらはStemline社にライセンスアウトしており、同社が臨床試験第1相を終了した段階で次の手を検討する予定でしたが、その段階に至るまでに時間がかかっていました。
XPO1阻害剤は、そもそも核内に存在するタンパク質を核外、つまり細胞質へ運び出す役割を持つタンパク質です。
それ自体は細胞にとって必要なタンパク質ですが、がん細胞においては核内にがん抑制因子や細胞周期阻害因子、転写因子など、がん細胞にとって不都合なタンパク質が多数存在しています。それらのタンパク質を核外に追い出すことで、生存するがん細胞が多く存在しています。
そこで、このXPO1で一時的に阻害すると、がん細胞が死滅するという仕組みになっています。
CBS9106の優位性

すでに上市済みのXPO1阻害剤「XPOVIO(Selinexor)」をKaryopharm社が販売していますが、それに対して「CBS9106」はより副作用を少なくできると考えており、「ベスト・イン・クラス」を目指しています。
XPO1は正常な細胞にも必要な作用を持つため、シャープに抑えたり、その抑制を停止したりできることが非常に重要です。それを実現できる可能性があると考えています。
CBS9106 ライセンス契約解消・全権利返還と今後

Stemline社には2014年にライセンスアウトし、2018年にその範囲を全世界に拡大しました。しかし昨年6月にすべての権利を当社に戻し、次の臨床試験を当社が進めることになっています。
基礎研究〜非臨床試験段階のプロジェクトの状況

基礎研究から前臨床試験準備段階のパイプラインは、スライドのとおりです。
2026年6月期2Qの業績 (1)損益計算書

加登住:2026年6月期第2四半期決算および財務状況についてご報告します。まず損益計算書です。これまでと同様に、事業収益の計上はありません。「CBP501」の臨床開発を中心に、研究開発投資を先行させている状況です。
事業費用は約6億円です。基礎研究費は前年とほぼ同等ですが、臨床開発費が例年より増加しています。
販管費は前年と同水準です。営業外損益については開示したとおりです。
事業費用は主に臨床試験関連費用で増減
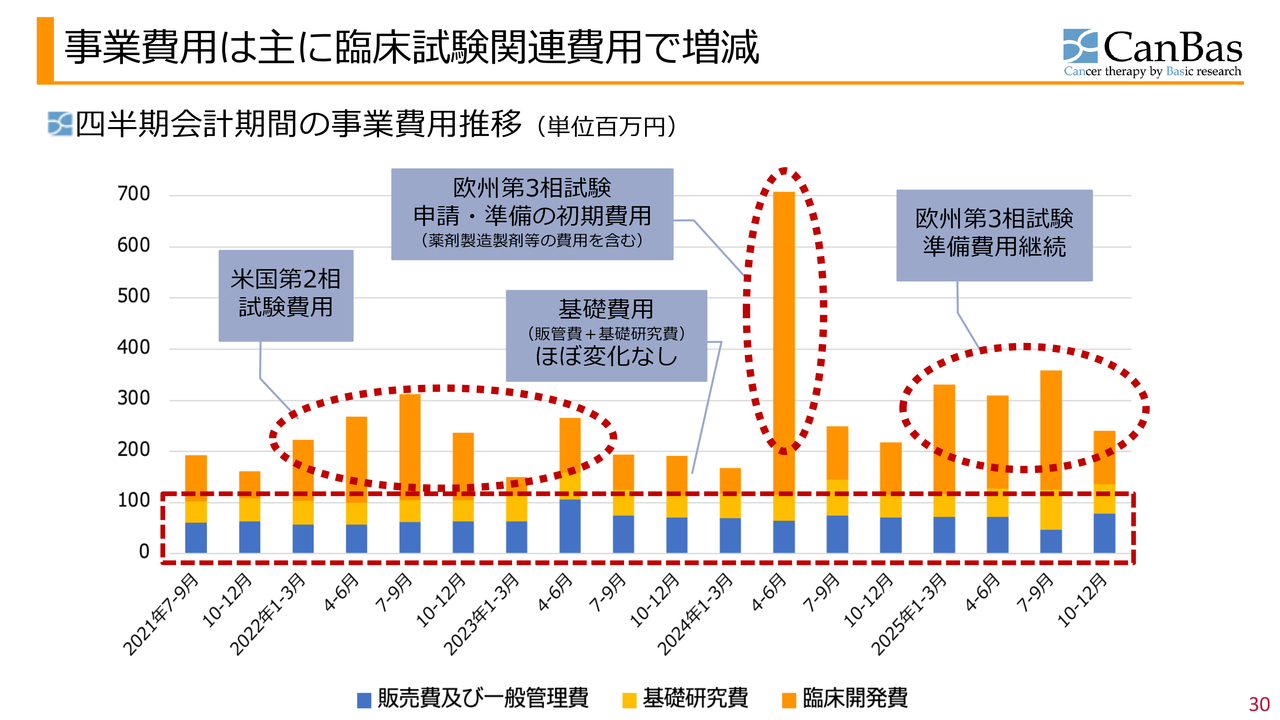
四半期ごとの事業費用の推移です。事業費用は、主に臨床試験の関連費用によって増減しています。スライドの図では、オレンジ色のグラフが臨床開発費を示しています。
2025年1月から9月までの期間は、臨床開発において、特に欧州での第3相試験の準備や規制対応のための製造関連費用を支出する時期が重なりました。そのため、四半期当たり約2億円の臨床開発費が発生しています。
一部の投資家のみなさまや決算書をご覧の方々から、「この状況が続くのならば、今のキャッシュで大丈夫なのか」といったご心配をいただいていました。この製造関連の規制対応費用等のピークは、ひとまず越えた状況です。2025年10月から12月の第2四半期会計期間については、臨床開発費は約1億円強となり、いったん落ち着いています。
2026年6月期2Qの業績 (2)貸借対照表の推移 (単位:百万円)
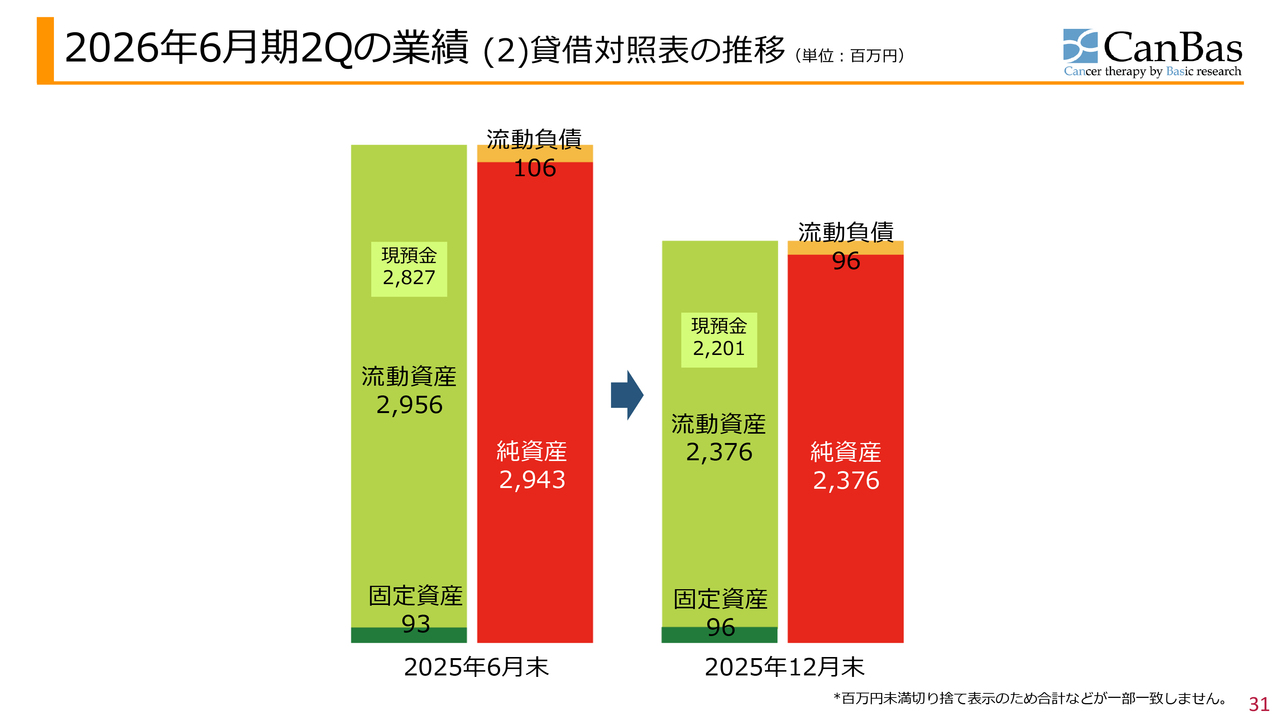
バランスシートです。当社の決算は単純で、キャッシュの減少分は事業費用と同程度になります。事業費用のマイナス分とキャッシュの減少分がそのまま反映されており、ほぼ同じだけバランスシートが縮小しています。
現預金については、昨年6月末は約28億円、昨年12月末では約22億円となっています。
四半期当たりでは、約2億円が販管費と基礎研究費、臨床開発費がそれ以上にかかる状況が続いています。
臨床試験の開始時期が遅れるとキャッシュの減りが少なくなるため、しばらく問題はありません。一方で開始時期が早まればキャッシュが一気に減少し始めるため、資金調達がなんらかのかたちで必要となります。
良いニュースがあればそれを踏まえて資金調達を実施し、良いニュースが来ない場合でもその間に慌てて資金調達を考える必要がある状況に当面ならない、という状況と考えています。
現在の企業価値評価に対するキャンバスの認識
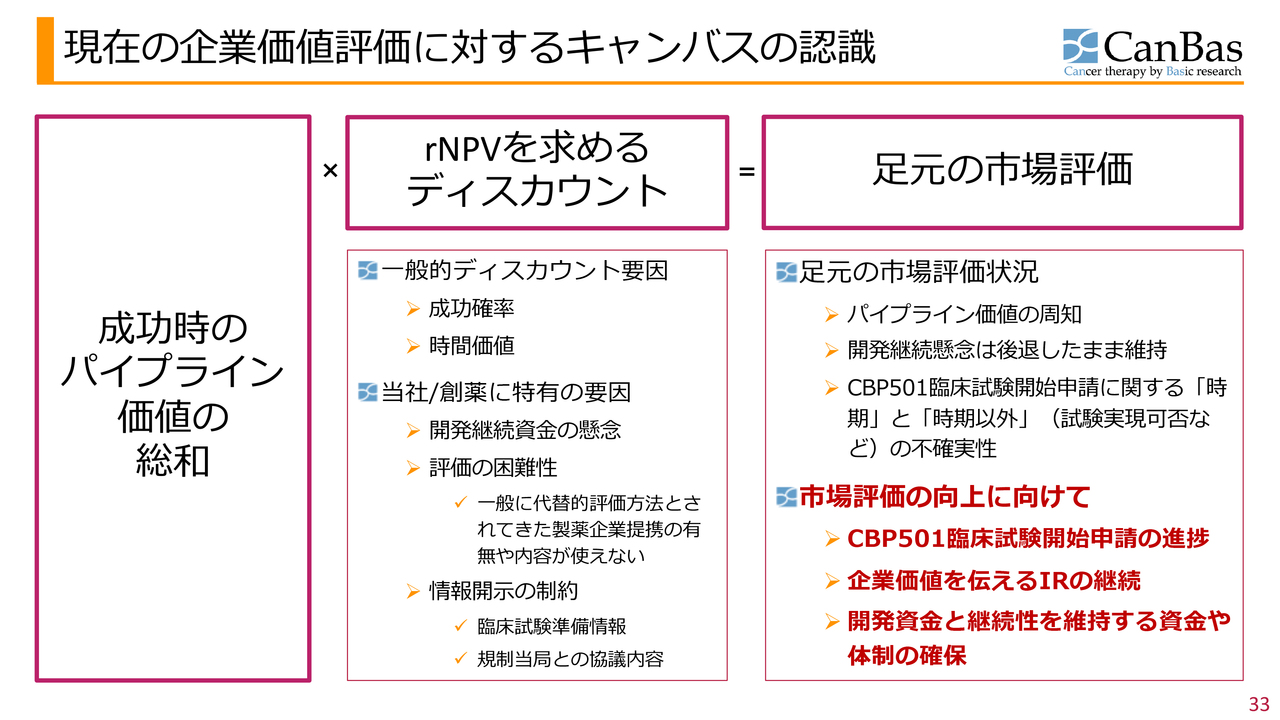
当社の株価や株式市場での評価については、現状ではキャッシュフローや利益、売上の成長ではなく、企業価値そのものを直接評価いただいていると考えています。さらなる向上を目指し、今後も施策を進めていきます。
当社では、成功時のパイプライン価値の総和とリスク調整後正味現在価値(rNPV)を求めるディスカウントの掛け算により、足元の市場評価が決まるという認識です。この向上のための取り組みについて、スライド右下に赤字で記載しています。
1つ目に、「CBP501」の臨床試験開始申請を着実に進めます。2つ目に、企業価値にご注目いただくためのIR活動を継続します。3つ目に、開発の進捗に応じて継続性を維持する資金体制の確保に注力します。
これら3つの施策によって、企業価値評価を継続的に高めていくことが可能だと考えています。今後も全力で取り組んでいきます。
現在のキャンバスの企業価値を評価する視点
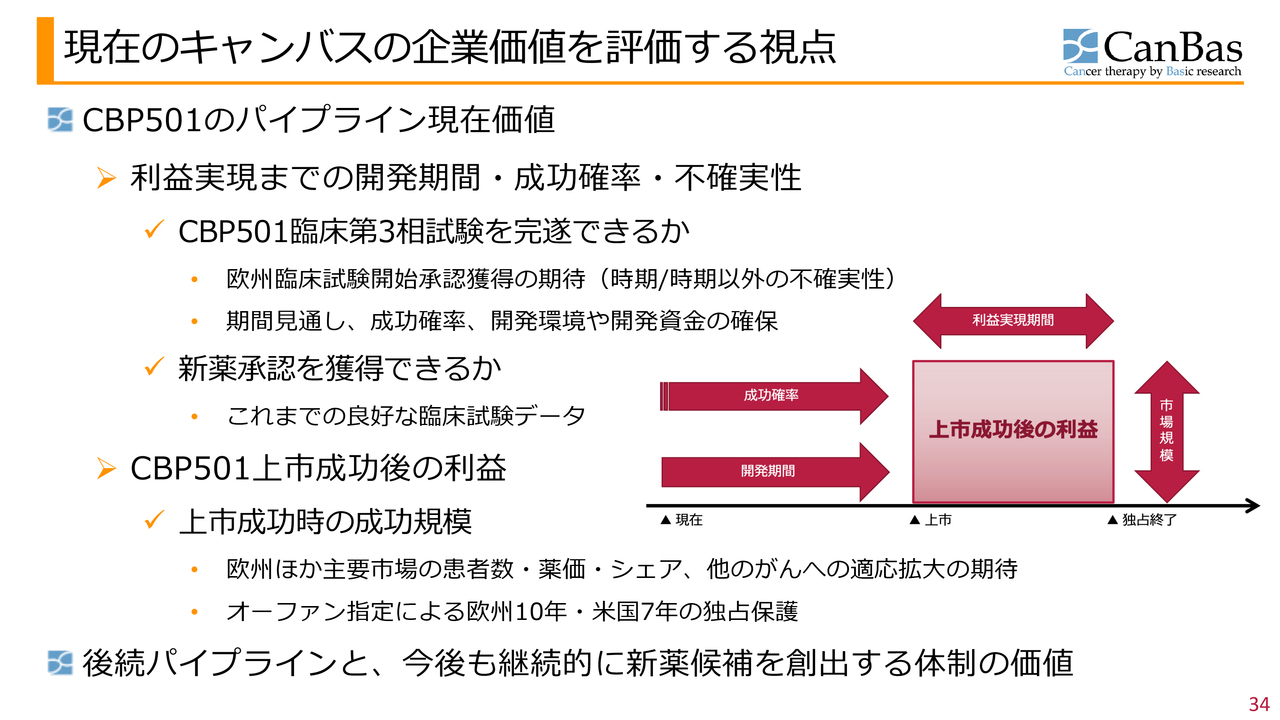
今お話しした内容を詳細に示したものがこちらのスライドです。「CBP501」のパイプラインの現在価値について、「利益実現までにどのくらいの期間がかかるのか」「成功確率はどの程度か」「不確実性はどうか」について記載していますので、ぜひご覧ください。
上市成功後の利益規模などについても、ニュースによって変化していきます。上市成功時の成功規模が間接的に現在価値に影響していることは言うまでもありません。
また冒頭にも申し上げたとおり、当社は「CBP501」のみに取り組んでいるわけではありません。今後も後続のパイプラインや、継続的に新薬候補を創出していき、きちんと企業価値の評価に反映させていくことが当面の課題と考えています。
開発資金確保に関する当社の現状認識

開発資金の確保についてです。2023年のファイナンスが成功裏に完了したことにより、現在も臨床試験の開始資金に問題はない状況です。
臨床第3相試験開始後の資金需要については、当初の見込費用から大きな変動はありません。追加の資本政策を検討する際には、株主価値の毀損や希薄化を可能な限り回避、または抑制する方法やタイミングを追求していきたいと考えています。
今後想定されるニュースフロー

今後想定されるニュースフローに変更はありません。「CBP501」関連では、欧州臨床第3相試験の開始承認の受領というニュースを、できる限り早く確実にお届けしたいと考えています。
「時期の不確実性」については、「いつよりも先だろう」とも「いつよりも前だろう」とも言えない状況です。この点に関して、「曖昧なことを言うな」といつもお叱りを受けますが、逆に曖昧なことを「不確実なこと」として示すことが、現状を最も正確に伝える方法だと考えて、この表現を使用しています。
「時期以外の不確実性」については予断を許さないものの、着実に減少しています。
その他についても、なんらかのニュースフローを作り出していきたいと考えています。
キャンバスの現状を知る情報源

キャンバスに関する情報源は、スライドのとおりです。
マーケットニュース

直近のニュースとして、東京証券取引所の「投資家が評価しているグロース上場企業の取組み事例集」に掲載されました。掲載された7項目のうち、スライドに記載の4項目で高評価をいただきました。
また2月13日に公表された「JPXスタートアップ急成長100指数」に、当社が選出されました。この配信は3月9日から開始される予定です。
これら2つのニュースは非常にありがたいことではありますが、手放しで喜んでいるわけではありません。
このように取り上げていただいたことで、私たちが常々お伝えしている企業価値が本当に正しいのかどうかを、これまで以上に厳しく問われる場面が増えると考えています。
また、より広い投資家のみなさまから注目やチェックを受ける状況になったという認識を持ち、より緊張感を持って今後の取り組みに当たっていきたいと思います。
質疑応答:薬剤製造規制対応と品質保証体制強化について
加登住:事前にいただいているご質問です。
「EMA(欧州医薬品庁)とのやり取りは、CMC(化学・製造・品質管理)に関するものだけでしょうか? その後、再び臨床開発そのものに関する課題が浮上したりしていませんか? 現在のやり取りの感触についてフォローアップをお願いします」というご質問です。
河邊:EMAとのやり取りについては、おっしゃるとおりです。これまで問題になっているのは薬剤の製造周辺に関することだけで、臨床に関してはいったんクリアされた状態と考えています。
時間がかかっていますし、臨床開発についても世界の状況が日進月歩ですので、今後臨床でなんらかの問題が生じる可能性はありますが、現状では特に懸念していません。
CMCに関しては、これまで「早期臨床から、最短で、最小金額で、必要最小限で物事を成す」の姿勢で進めてきましたが、後期臨床から市販を目指す段階では、重層的な品質保証や安全性対策が必要となっています。
そのため、EMAとのやり取りに時間がかかるだけでなく、当社自身の体制も強化しており、品質保証に関する仕組みを非常に厚くしてきているところです。
質疑応答:製造委託業者の移転や切り替えの可能性について
加登住:こちらも事前にいただいているご質問です。
「製造関係の細かい問題等で時間がかかっているということであれば、これを克服するために、そのような問題が発生しない製造委託業者への製造の移転、もしくは欧州での製造への切り替えといった対応の選択肢はお考えでしょうか?」というご質問です。
これについては「X」でもすでに質疑のやりとりがありましたので、私から回答します。
ご指摘のとおり、これまでの蓄積もあるため、元の製造委託先で修正対応するのが最も迅速であると認識しています。この可能性を追求するのと並行して、プランBも検討しています。
プランBとして、時間と技術移転にリスクが伴うものの、それをクリアすれば承認取得の確度が上がる可能性があるという観点から、欧州、もしくは欧州でのノウハウや歴史を持つ会社への移管を進めることも考えています。こちらを並行して進めることも考慮できます。
昨年以降、「どのようなリスクやデメリット、メリットがあるか」について、社内で比較検討しています。「X」でも回答したとおり、実際に変更した点などの情報については、公開できない内容や情報が含まれるため、当社としては開示の対象外としています。この点についてはご理解いただければと思います。
いずれにしても、実現したいことは「最も短い期間で」「最も確実に」の両立です。多少コストや時間が多くかかったり、回り道になったりする場合でも、「確実かつ早期」という目標を達成するためであれば進めていくという方針を継続しています。この点についてご理解いただければと思います。
質疑応答:他社の免疫着火剤と膵臓がん治療薬の開発状況について
加登住:あらかじめいただいている最後のご質問です。
「他社でも免疫着火剤、すなわち免疫ホットの概念をターゲットとしたアプローチで開発が進められているようです。こちらの他社の開発状況と、膵臓がんという観点での他社の最新の開発状況にアップデートがあれば教えてください。
また免疫着火剤は、がんの微小環境においてどのように働き、がん免疫をどう再活性化するか、メカニズムごとにタイプが分かれていると考えられていますが、『CBP501』は他のどのタイプと類似し、どのタイプに分類されるのでしょうか?」というご質問です。
河邊:他社の免疫チェックポイント阻害剤に関連する取り組みや膵臓がん関連の開発については、臨床試験の第1相試験や第2相試験の前半段階で非常に多くのプロジェクトが進行しています。その多くが「有望かもしれない」と言われながら姿を消していくという過程を繰り返しています。
そのような中で、後期臨床となる第3相試験を大規模に実施しているものとして、活性型RASを阻害する薬剤が挙げられます。この薬剤は膵臓がんに対する臨床試験も進められており、第2相試験でも良好な結果を出し、有望と考えています。
競合という観点では、私たちは競合にはならないと考えています。もし臨床試験で完全に治癒する薬が登場すれば別ですが、そうでない場合、患者さまは良い状態を維持しながらも、いずれ進行したがんに対して薬剤が必要になると考えています。
現在、膵臓がんの3次治療をターゲットとしている「CBP501」に関しては、むしろ3次治療に来る患者さまの状態が、従来よりも良い状態で来る可能性が高くなると考えています。その結果、対象となる患者数が増加する方向に作用すると見ています。
また免疫に関わる分子は非常に多岐にわたり、それぞれの段階やステップも多いため、分子として標的となるものが多数存在します。
それぞれについて阻害剤や活性化剤が開発されており、早期臨床試験が進行中です。その種類は非常に多く、言い尽くせないほど数多く存在します。
私たちの「CBP501」の特徴は、1つの分子を強く動かすものではなく、全体として働くタイプであるという点にあります。
免疫系はご存じのとおり、大きな刺激を受けると必ずそれを抑えるために逆の働きを体内で行い、バランスを取ろうとする強い特性を持っています。
その中で「CBP501」は、がん細胞が死ぬ際に、免疫細胞がそれに気づけるような免疫原性細胞死を導くことによって、そもそもの免疫反応の開始部分を力強く刺激します。
また免疫抑制的なマクロファージなどを阻害することで、そのマクロファージが産生する「IL-10」や「IL-6」など免疫抑制的なサイトカインがあります。それぞれを阻害する薬剤の開発は欧米の企業が試みていますが、私たちの「CBP501」は、それら全体をゆるやかに抑えるという作用を持っています。
この点で、他社と私たちが目指すところは大きく異なっています。同じように免疫に最初の着火を行うという役割であっても、その着火の方法がまったく違うというものになります。
言い方を変えれば、シャープな方法の欧米に対し、全体としてぼやっとしているように見えるかもしれませんが、免疫系のカウンター作用や緩衝作用が強いことを考えると、この「ぼやっとしている」ものが案外とよく効くと私たちは考えています。
質疑応答:第3相試験のインクルージョン・クライテリアについて
質問者:今回の第3相試験のインクルージョン・クライテリア(組入基準)に関してご質問です。現在、いわゆるPan-KRAS阻害薬や、最近siRNAなども臨床試験で検証されていると思います。このような治験に参加された患者さまもインクルージョンできるデザインになっているという理解でよろしいでしょうか?
河邊:2種類以上の治療を受けた患者さまはすべて対象となります。前に受けた臨床試験が終わってから一定期間が経過していれば問題ありません。
質問者:またADC(抗体薬物複合体)に関してもかなり多く組み込まれている印象を受けるのですが、それについてもまったく問題ないという理解でよろしいでしょうか?
河邊:おっしゃるとおりです。ただし、膵臓がんにおいては残念ながらADCも十分な効果を示さないことが多いため、受けている患者さまは少ないと思いますが、対象に含まれます。
質問者:クライテリアとしては2例以上の治療を受けた患者全体という理解でよろしいですか?
河邊:そのとおりです。
質問者:とにかく、早く始められることが重要ということですね。
河邊:おっしゃるとおりです。
この銘柄の最新ニュース
CANBASのニュース一覧- 2026年6月期 第2四半期決算説明会資料 2026/02/18
- 2026年6月期 第2四半期(中間期)決算短信〔日本基準〕(非連結) 2026/02/13
- 営業外損益の計上に関するお知らせ 2026/02/13
- CANBAS、上期経常が赤字拡大で着地・10-12月期も赤字拡大 2026/02/13
- 前日に動いた銘柄 part2 エイチエムコム、東祥、イーディーピーなど 2026/02/05
マーケットニュース
- 対米投資候補として脚光再び、騰勢前夜の「アンモニア」関連株を追う <株探トップ特集> (02/25)
- 明日の株式相場に向けて=復活の鐘を鳴らすレアアース関連 (02/25)
- 25日香港・ハンセン指数=終値26765.72(+175.40) (02/25)
- 欧米為替見通し: ドル・円は伸び悩みか、円売り継続も高値では介入に警戒 (02/25)
おすすめ条件でスクリーニングされた銘柄を見る
キャンバスの取引履歴を振り返りませんか?
キャンバスの株を取引したことがありますか?みんかぶアセットプランナーに取引口座を連携すると売買履歴をチャート上にプロットし、自分の取引を視覚的に確認することができます。
アセットプランナーの取引履歴機能とは
※アセプラを初めてご利用の場合は会員登録からお手続き下さい。



