【QAあり】サスメド、強固な財務基盤のもと投資を継続 臨床試験システムの追加機能や不眠症治療アプリ等で収益拡大を目指す
ビジョン
上野太郎氏(以下、上野):サスメド株式会社代表取締役社長の上野です。本日はお時間をいただきありがとうございます。それでは、スライドに沿ってご説明します。
まず、弊社のビジョンです。「ICTの活用で『持続可能な医療』を目指す」をビジョンに掲げ、その意味である「SUStainable MEDicine」を略してサスメド株式会社と称しています。
事業領域概要
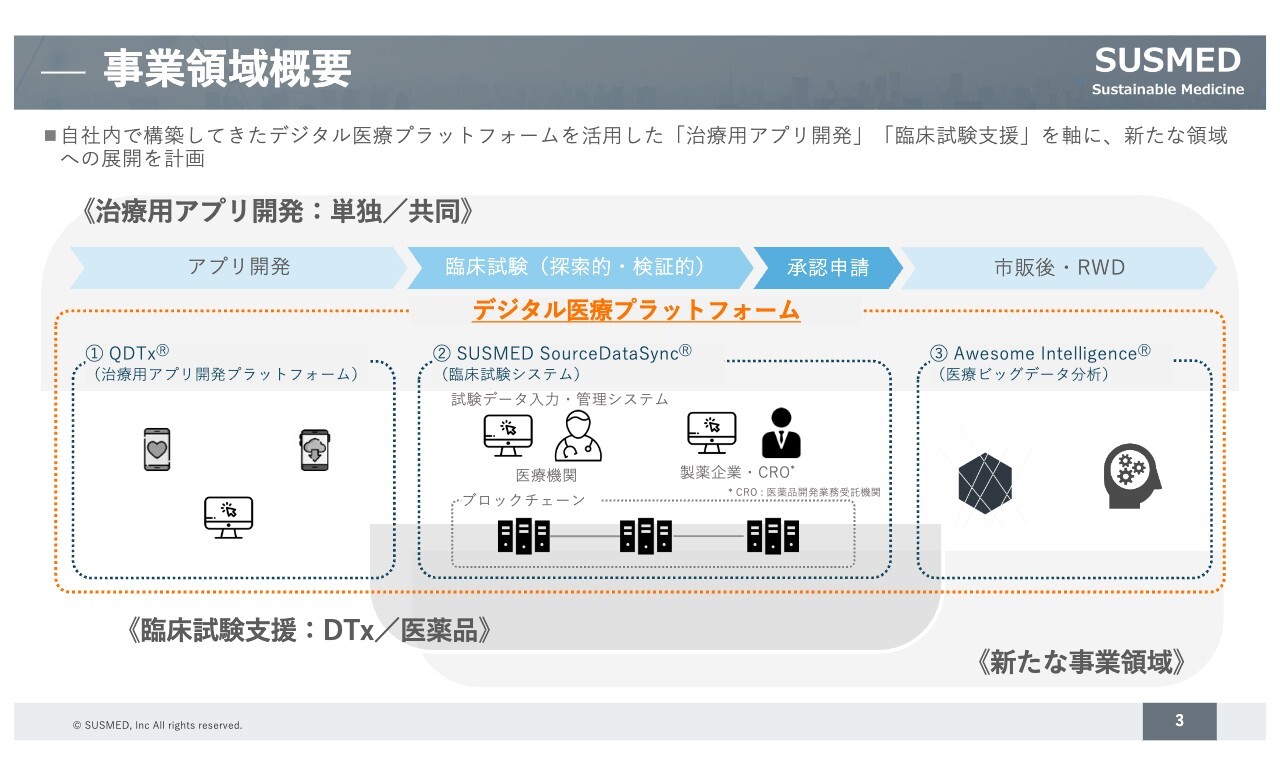
具体的な取り組みの全体像をスライドに示します。弊社が有するデジタル医療プラットフォームを活用することにより、弊社単独あるいは製薬企業と共同で、治療用アプリの迅速な開発を進めています。
治療用アプリのみならず、医薬品も含めて治験の効率的な実施のための技術基盤となる臨床試験システムを、私どもは「SUSMED SourceDataSync」と呼んでいます。このシステムを自社で活用したり、共同開発の中で使用したり、製薬企業に提供したりしています。
このようなデジタル技術を医療の中で使うことで、医療データをより取得しやすくなります。取得した医療データの活用を見越して医療ビッグデータを分析する取り組みも、当社のプラットフォームを活用して行っています。
QDTx:治療用アプリ開発プラットフォーム
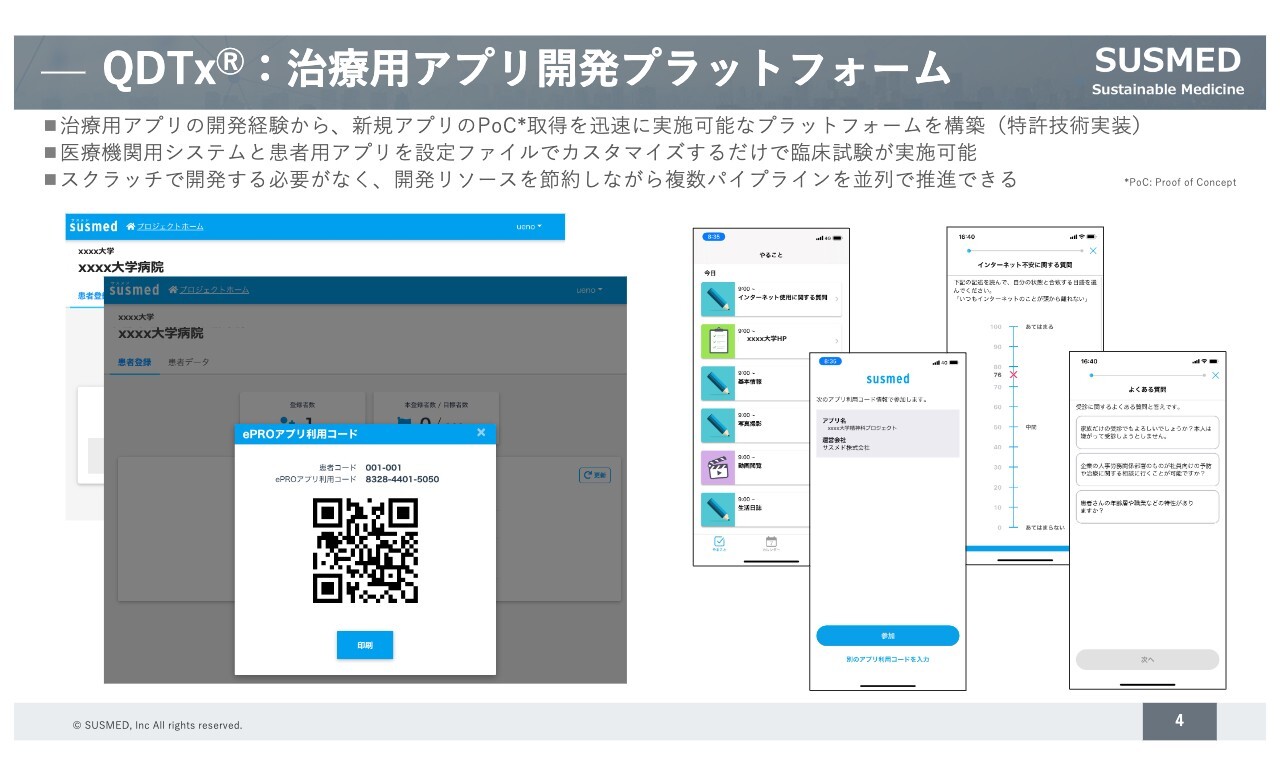
それぞれのプラットフォームについて、簡単にご説明します。「QDTx」は治療用アプリの開発プラットフォームです。これまでの治療用アプリの開発経験から、新しい治療用アプリを迅速に開発できるプラットフォームを特許技術を実装して構築しています。
「QDTx」は、スマートフォン向けアプリのみならず、治験を行う際の医療機関側での管理システムを連動して立ち上げる仕組みになっています。こちらを活用することで、エンジニアがゼロからスクラッチで開発することなく、複数パイプラインを並列で迅速に推進できます。
後ほどご紹介しますが、こういったプラットフォームの機能が、弊社のような規模の会社でも、複数パイプラインを並列に開発できる背景になっています。
SUSMED SourceDataSync:臨床試験システム

臨床試験システムの「SUSMED SourceDataSync」です。SDSと略していることもあります。弊社はブロックチェーンの技術を臨床試験に用いる特許を有しており、こちらを実装したシステムです。
治験を実施する際にはレギュレーション上、データの信頼性の担保が求められており、通常はCRO企業の方々が労働集約的に照合作業などを行うことで信頼性が担保されています。弊社のブロックチェーン技術を使うことで、レギュレーションを遵守しながらシステムでこの照合作業を代替することができるという仕組みになっています。
こちらは弊社の治療用アプリの開発の中で活用することもありますし、共同開発の中で使用したり、医薬品の治験などでも活用していただいています。
後ほどご紹介しますが、現在、治験以外のところでもブロックチェーンシステムの活用が広がってきています。
Awesome Intelligence:機械学習自動分析システム
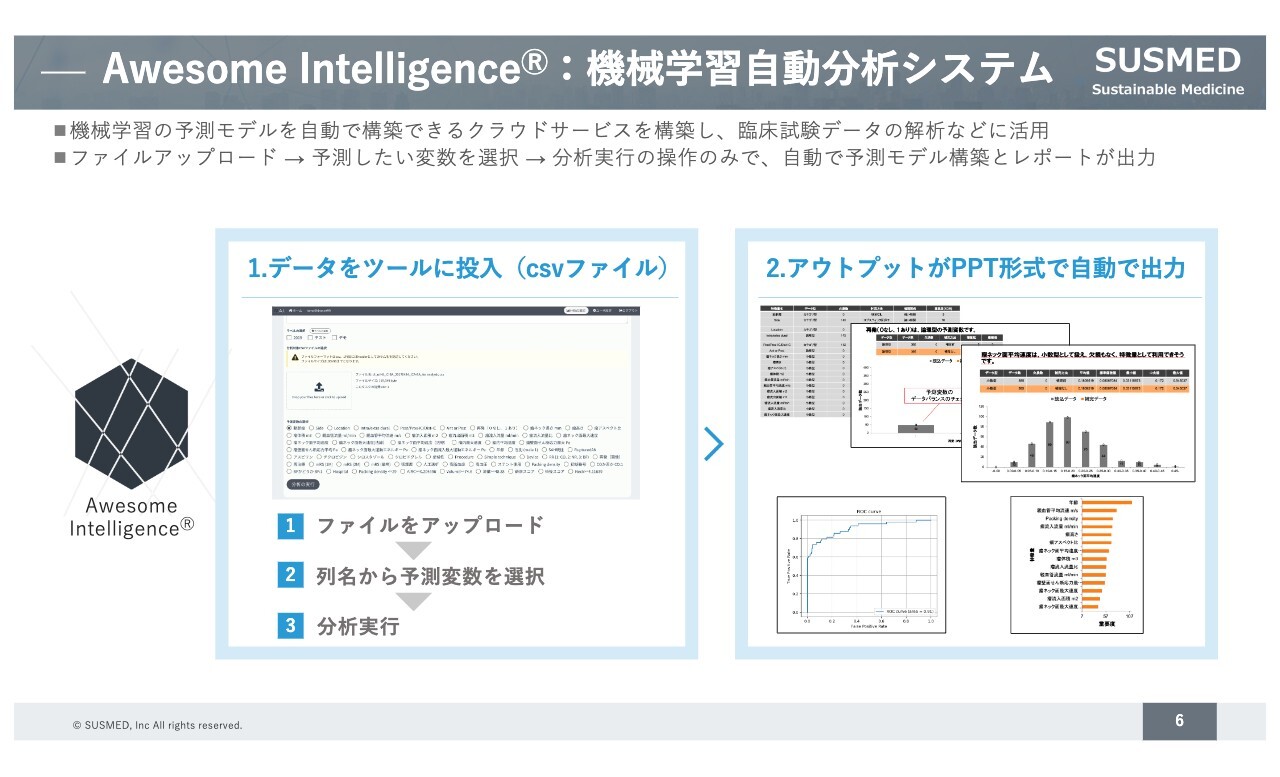
「Awesome Intelligence」は、医療ビッグデータを分析するための基盤システムです。クラウドベースで機械学習のデータ分析を行える仕組みになっており、この技術を使うことで、製薬企業やアカデミアがすでに保有しているデータを機械学習で分析して予測モデルを構築するという取り組みを行っています。
今後、治療用アプリを上市した際には、治療用アプリ経由でビッグデータが集積されますので、これらのデータの利活用を見据え、基盤との連携を予定しています。
治療用アプリの提供の流れ
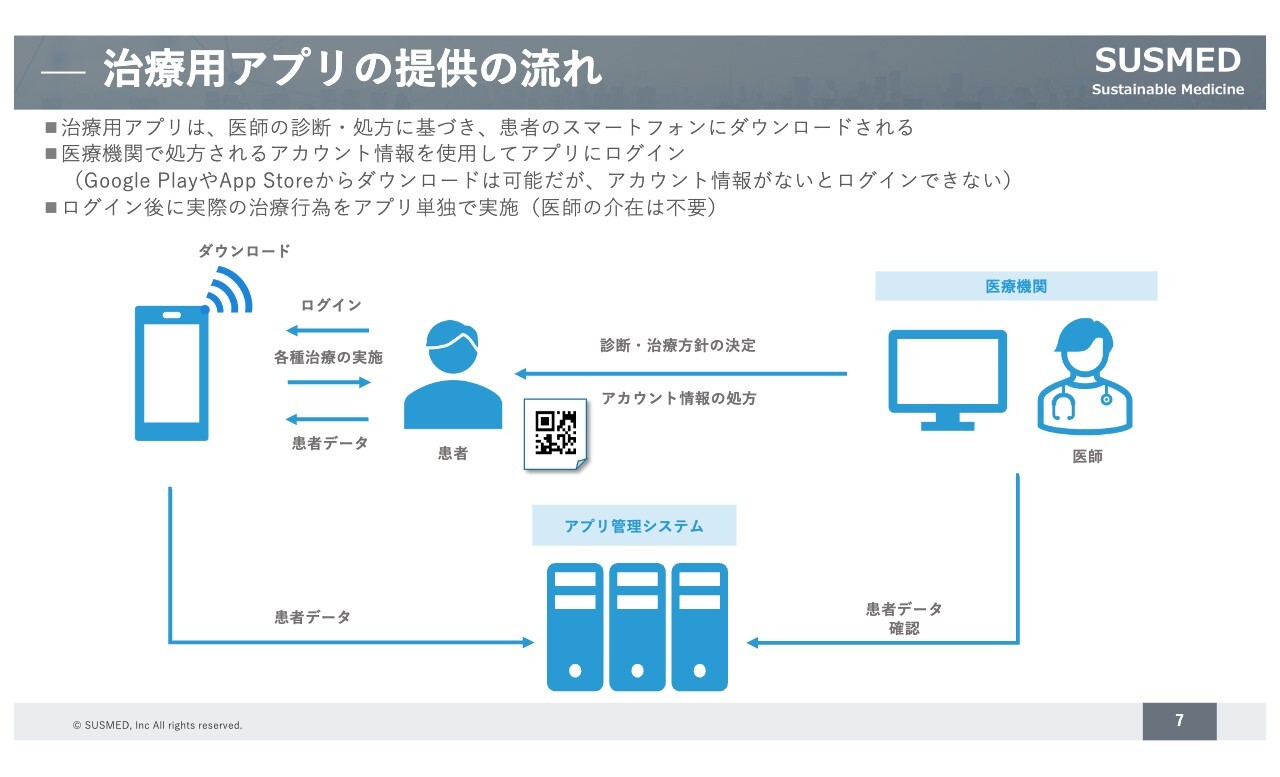
弊社が取り組んでいる治療用アプリ分野についてご説明します。ご存じの方もいらっしゃるかと思いますが、治療用アプリは医療機器に該当しますので、医師の診断・処方に基づいて患者さまのスマートフォンにダウンロードされ、自宅での治療に使うかたちになります。
アプリへのログインは、医療機関で処方されるアカウントを利用することではじめて可能になるという仕組みです。
ログインした後は、患者さまのスマートフォンを用いて自宅で治療を受けるかたちになりますので、日々患者さまのデータがサーバーに集まってくる点も新しいところです。このデータをサーバー経由で医療機関で確認し、治療方針の策定などにも活用します。
遠隔医療などとは異なり、アプリ単独で治療することになりますので、治療の各ステップに医師の介在は不要となっています。
ヘルスケアアプリと治療用アプリの違い
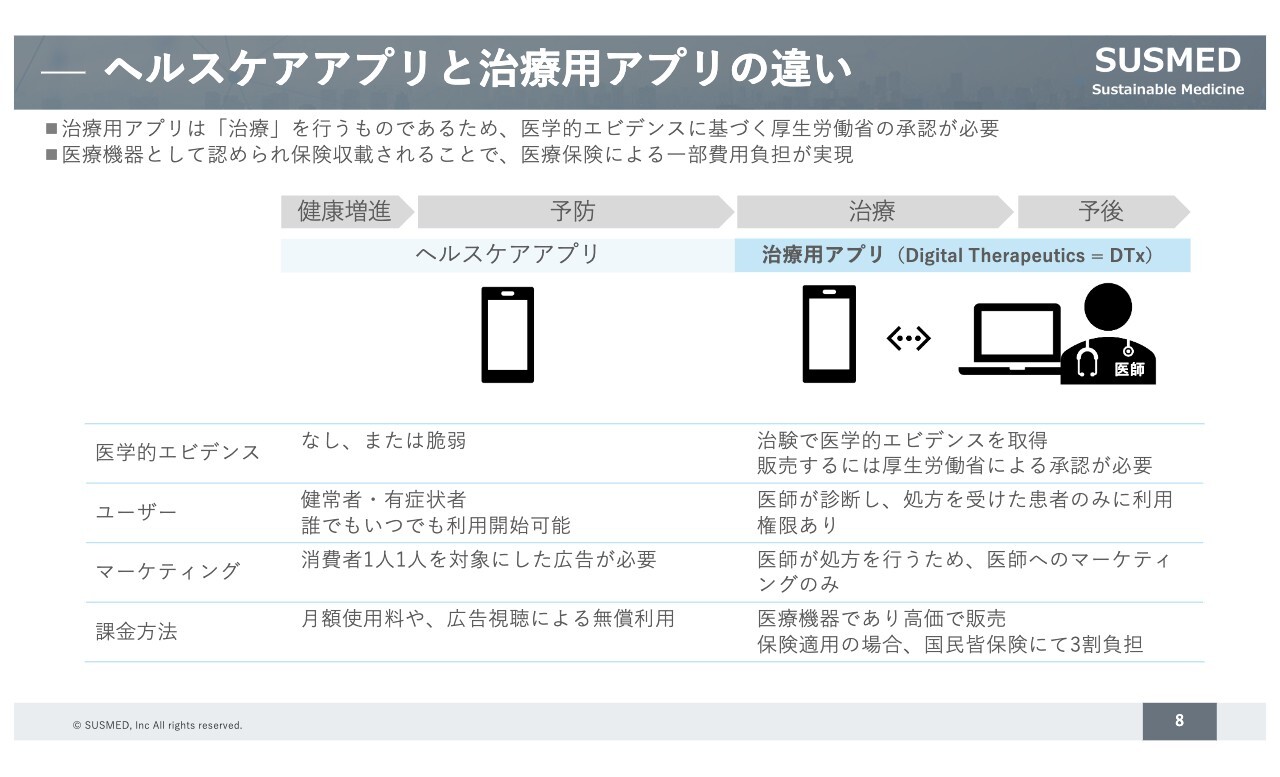
こちらもご存じの方が多いかと思いますが、今、世の中に多数あるヘルスケアアプリとの違いをご説明します。ヘルスケアアプリはあくまで健常者が使うため、疾患の診断や治療ができると謳うことはできません。
一方で、治療用アプリは医療機器に該当しますので、医薬品や医療機器と同じように、治験でエビデンスを得た上で承認を取得することにより、はじめて販売できます。保険制度も活用できますので、私どもも保険適用を目指して各プロダクトの開発を進めています。
開発パイプライン① (2024年8月9日現在)
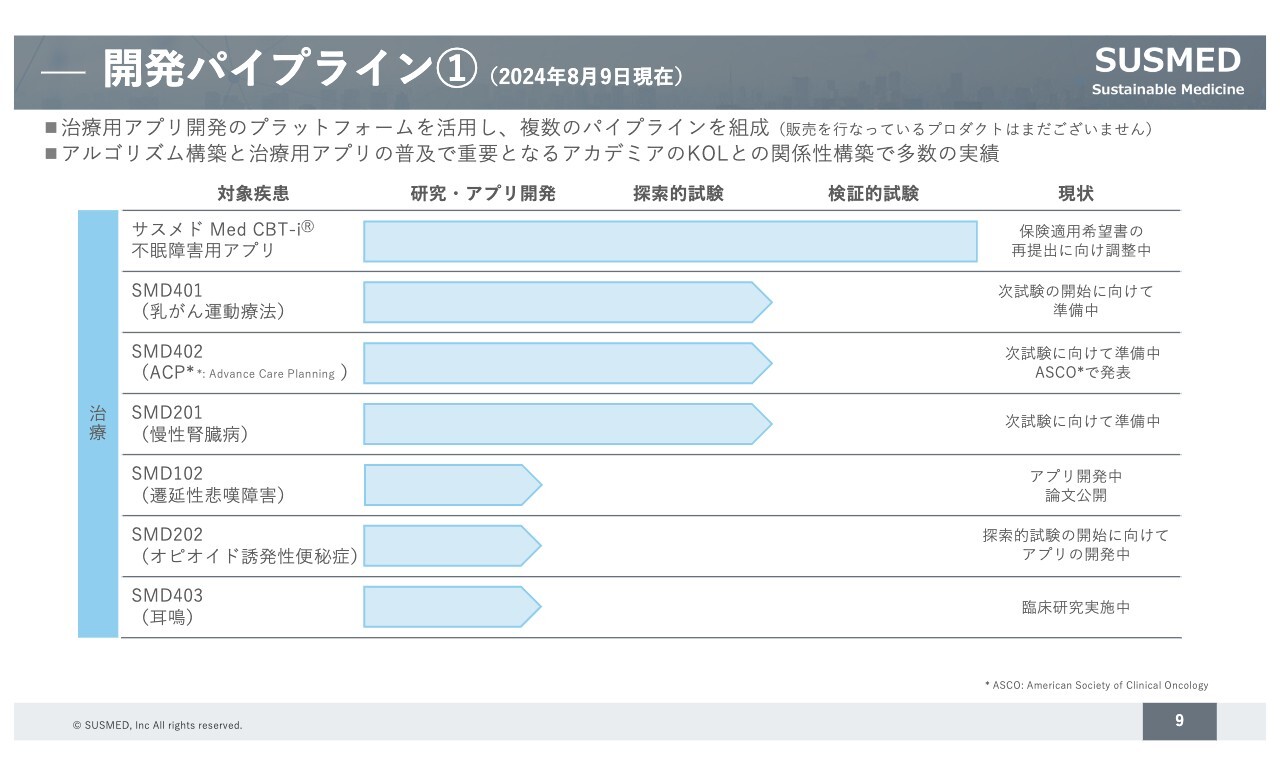
弊社が抱えているパイプラインです。弊社単独で開発しているもののほか、製薬企業と共同開発しているものも示しています。
不眠症の治療アプリについては、保険適用に向けて取り組みを進めています。そのほかに開発が進んでいる「SMD401」「SMD402」「SMD201」については、次試験に向けての取り組みが進んでいる状況です。
製薬企業との取り組みでは、耳鳴の治療用アプリを杏林製薬と一緒に開発中です。今、特定臨床研究を実施しています。
開発パイプライン② (2024年8月9日現在)
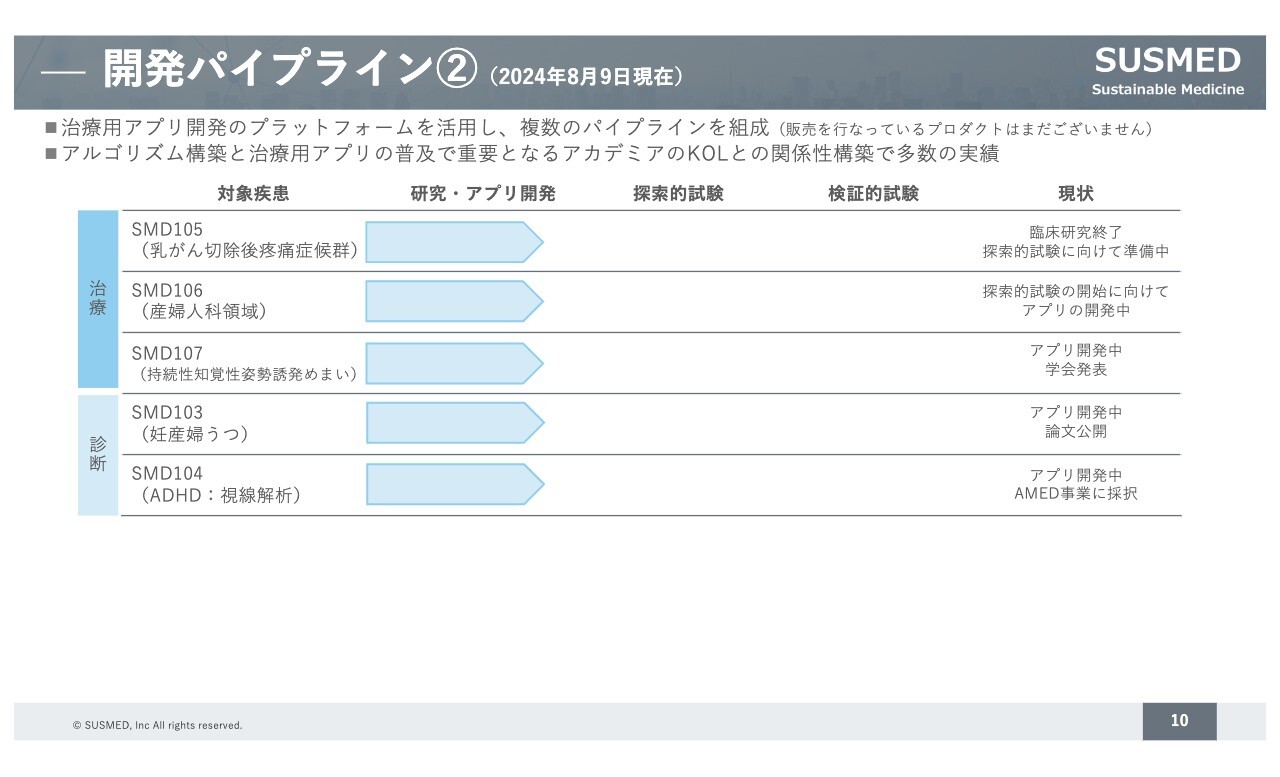
パイプラインの続きです。「SMD106」はあすか製薬との共同開発になります。こちらは臨床試験の開始に向けて取り組んでいる状況です。
治療用アプリのほか、妊産婦のうつや発達障害であるADHD向けの診断用アプリの開発を進めています。
2024年6月期 重点施策

前期、2024年6月期の重点施策は4点ありました。
1点目は不眠障害治療用アプリの販売開始、2点目は後続パイプラインの開発です。
3点目と4点目はプラットフォーム関連で、臨床試験システム活用の部分となります。臨床試験システムの新規案件の獲得に加え、治験以外のところでこの技術を活用することにも取り組んでいます。具体的にはレジストリというもので、承認・上市以降の医療ビッグデータのデータ管理の仕組みにブロックチェーン技術を用いるという取り組みです。
重点施策①不眠障害治療用アプリの販売開始
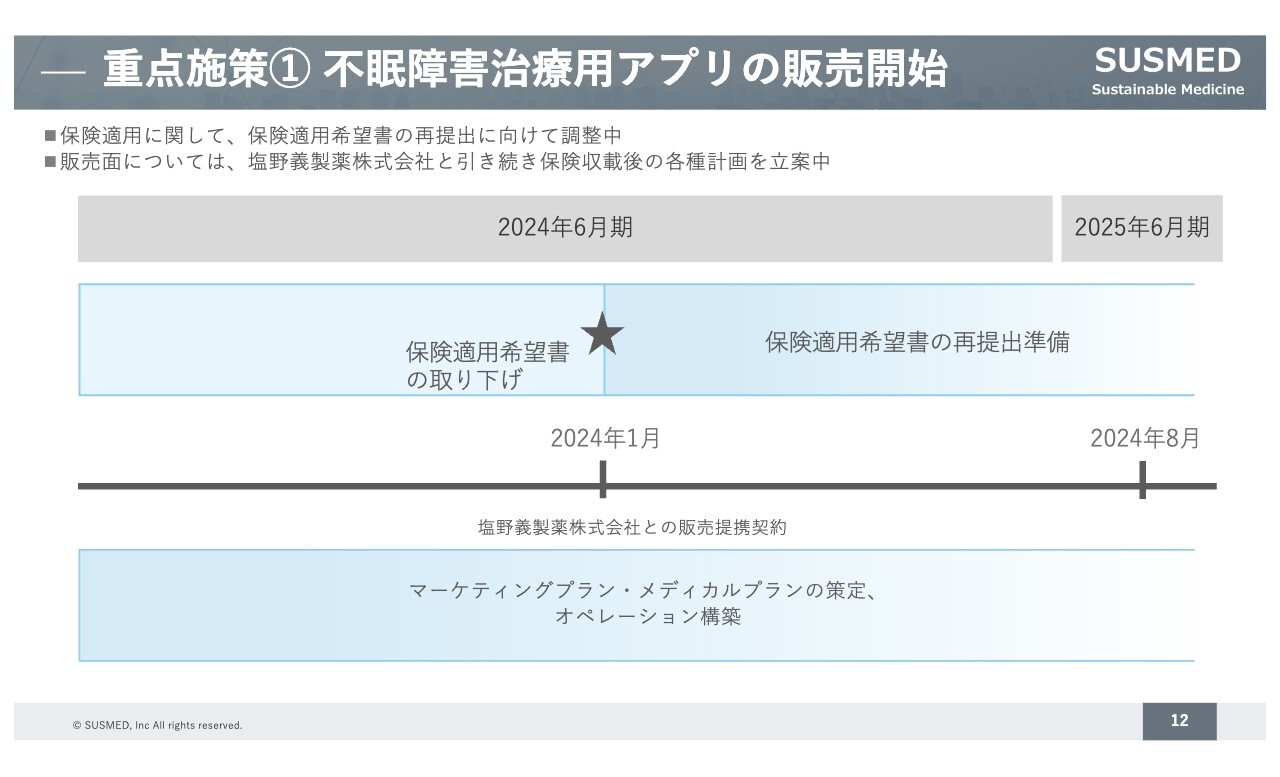
それぞれの進捗についてご紹介します。不眠障害治療用アプリの販売開始については、2024年1月時点で保険適用が見送りになりましたので、保険適用希望書をいったん取り下げました。制度変更に応じた保険適用希望書の再提出に向け、調整を進めています。
販売面については、塩野義製薬と販売提携契約を結んでいますので、引き続き保険収載後の販売計画などの具体化を進めている状況です。
2024年6月期 重点施策の進捗状況

その他の重点政策の進捗については、スライドに記載のとおりです。
後続のパイプラインについては、実際に臨床試験を実施して次のステップに進んでいるものだったり、先ほどお伝えしたように製薬企業との取り組みとして特定臨床研究を開始するといったことを行っています。
ブロックチェーン技術を使った臨床試験システムについては、耳鳴の治療用アプリの特定臨床研究で使用中です。すでに稼働していた医薬品の臨床試験に加えて、このような新規案件を受注しています。
レジストリについては、静脈疾患レジストリの構築に関する基本合意を締結し、実際の構築に向けた取り組みを進めている状況です。
業績ハイライト
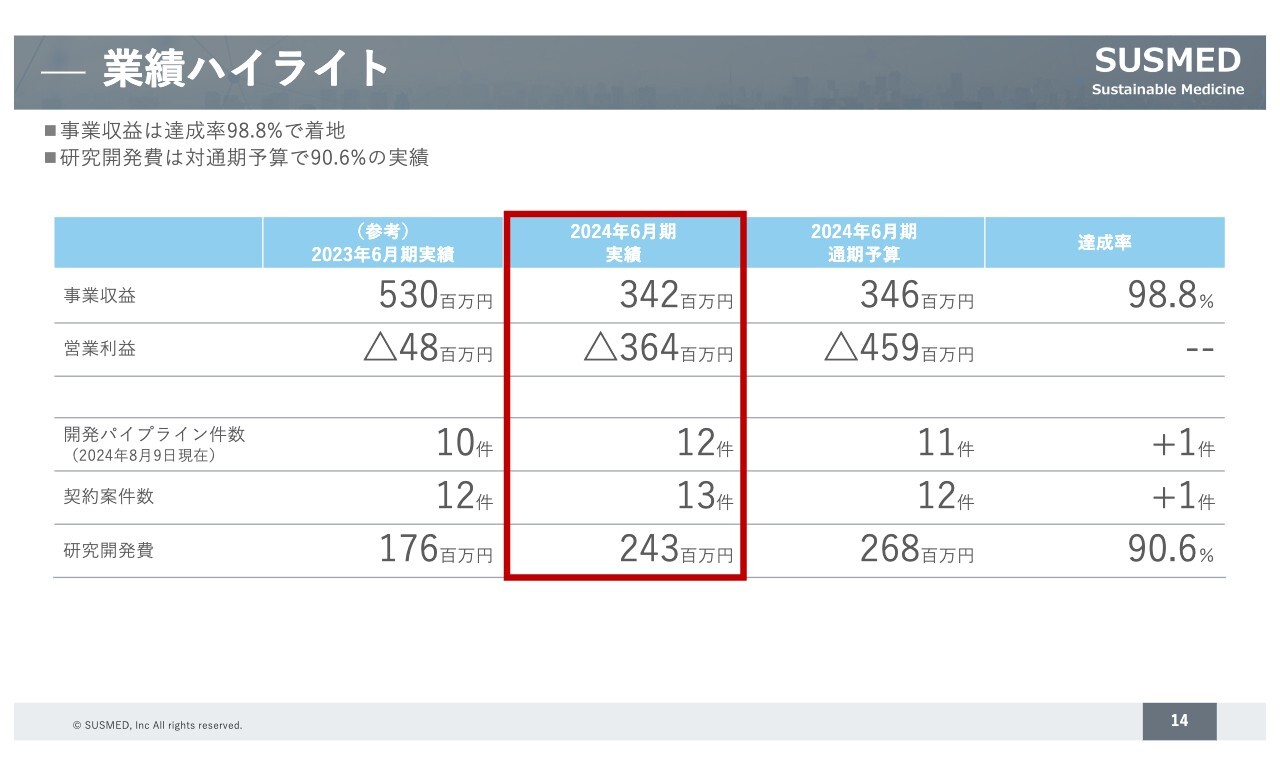
業績面についてご説明します。前期の事業収益は3億4,200万円で着地しました。予算は3億4,600万円だったため、400万円ほどショートしたかたちです。
一方、販管費で圧縮できた部分もあり、営業利益はマイナス3億6,400万円となっています。研究開発を進めることで、研究開発費で2億4,300万円を使用しました。
セグメント業績
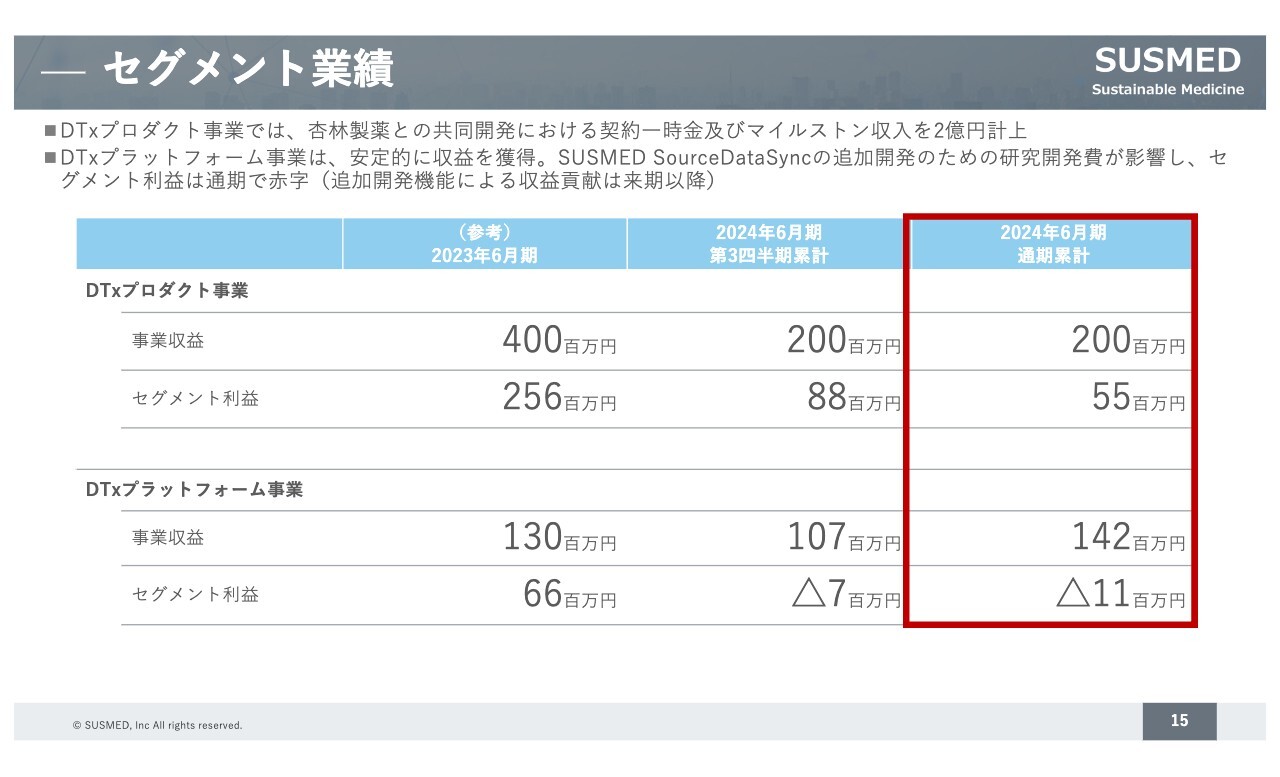
セグメントごとの実績です。DTxプロダクト事業については、杏林製薬との耳鳴の治療用アプリ開発においてマイルストン収入が売上計上されたため、事業収益は2億円となりました。
DTxプラットフォーム事業については、安定的に収益を獲得していますが、追加開発を行っているため、セグメント利益は2023年6月期の黒字に対して赤字となっています。前期で追加開発した機能は、2025年6月期以降、収益に貢献していくと考えています。
財務状況
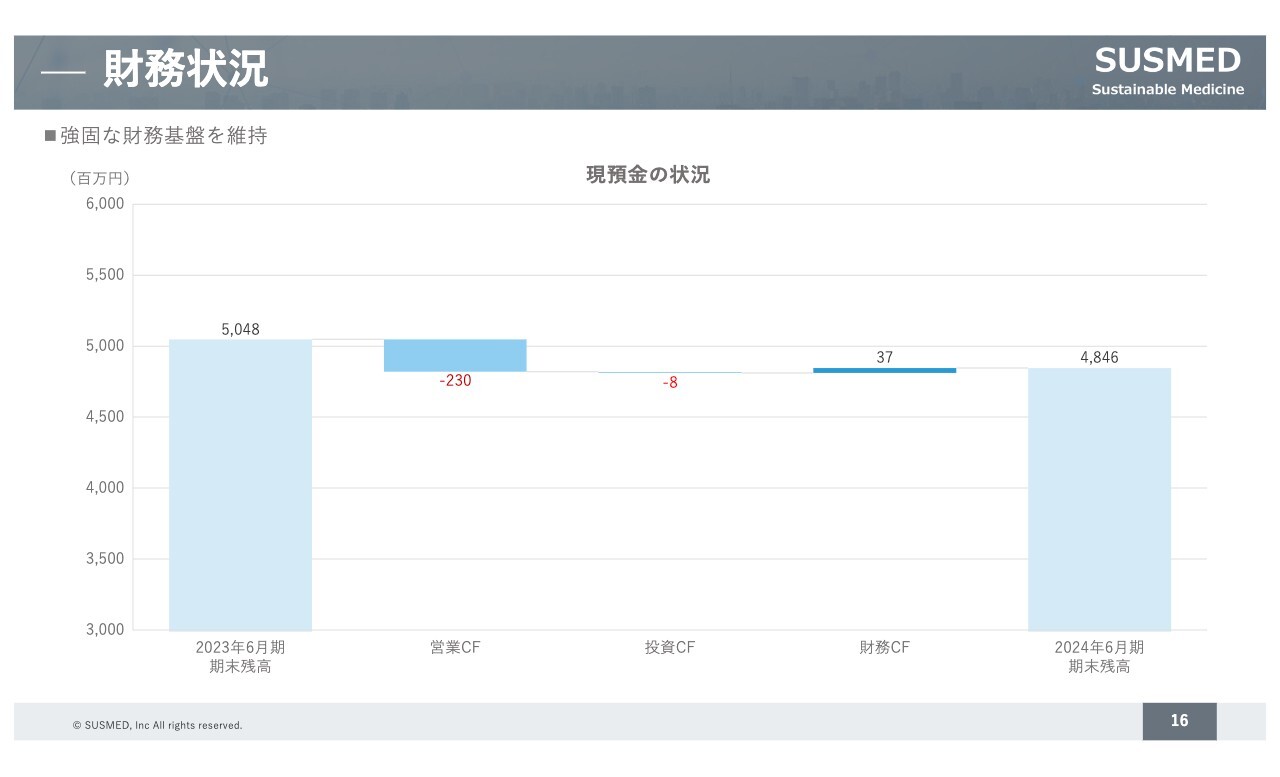
財務状況はスライドに記載のとおりです。強固な財務基盤を維持しています。
2025年6月期業績予想
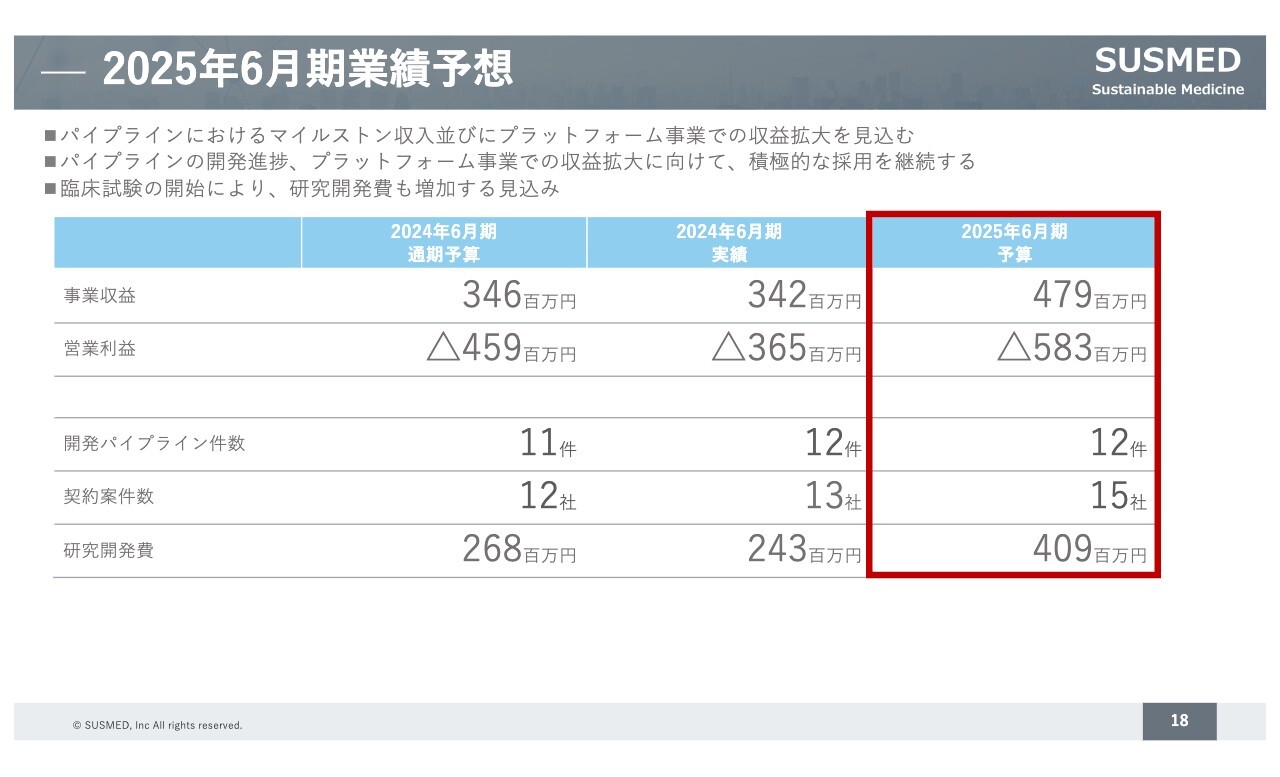
2025年6月期の業績予想をご説明します。パイプラインにおけるマイルストン収入とプラットフォーム事業での収益拡大を見込んでいるため、事業収益は4億7,900万円を計画しています。
一方で、採用活動を進めたり、研究開発に前期以上にしっかりと投資して後続のパイプラインの開発を進めていくため、営業利益はマイナス5億8,300万円を見込んでいます。
2025年6月期 重点施策

2025年6月期の重点施策です。不眠障害治療用アプリについては、保険収載に向けた取り組みを引き続き進めていきます。
パイプラインの開発進捗についても、前期から継続して各パイプラインの開発を進めていきます。これまで開発してきたものに加え、新しくパイプラインとして追加されたものもありますので、それぞれの臨床開発を進めていくことを掲げています。
プラットフォームについては、今後、臨床試験システムの使用事例を横展開することで案件の獲得を増やすことを予定しているため、複数試験での稼働を掲げています。
レジストリへの展開については、前期から構築している静脈疾患レジストリシステムの稼動を今期中に実施することを掲げています。
私からの決算説明は以上です。
質疑応答:保険収載の現況について

質問者:今期の重点施策について、1つ目に「不眠障害治療用アプリの保険収載」と記載されています。
現時点では保険適用希望書を出していないと認識していますが、今期の残り10ヶ月から11ヶ月ほどで保険収載の見通しが立っているということでしょうか? あるいは、単純に目標として掲げているということでしょうか? どの程度の確度で掲げているかを教えてください。
上野:前期からお伝えしているように、省庁の方々とコミュニケーションを取りながら、保険収載に向けた話し合いを進めてきています。
一方で、タイミングについては、当然ながら私どもも確たることはお伝えできませんが、話し合いの進捗状況から、弊社の重点施策として不眠障害治療用アプリの保険収載を掲げているかたちです。
質問者:保険適用希望書の提出時期について、上期になるのか、下期になるのかなどのコメントはいただけますか?
上野:開示すべき事項が生じた時点で開示させていただく予定でおり、現時点で私どもから時期などをお伝えすることはできかねます。
質問者:保険適用希望書の提出にあたり、規制当局から課題が出ているなど、ハードルがあるわけではないという認識でよろしいでしょうか?
上野:規制当局の方々とは継続的にお話ししています。従前お伝えしているように、今年6月に制度変更があり、その制度の下での必要な手続きについてコミュニケーションを取ってきているかたちです。規制当局とのやり取りの中では、保険収載について明確に「できない」という状況は、現時点では発生していません。
質疑応答:不眠障害治療用アプリのマイルストン収入について

質問者:今期の業績予想で、事業収益は5億円弱を計画しています。私の認識では、治療用アプリにはマイルストンが設定されていると思います。不眠障害治療用アプリに関するマイルストン収入は今期の計画に入っていますか?
上野:パイプラインにおけるマイルストン収入については、事業収益5億円弱の中に含まれていますが、どのプロダクトに起因するものかについては開示していません。
質疑応答:セグメント別の業績予想について
質問者:具体的な数字はけっこうですが、今期業績予想について、事業収益5億円弱のうち、DTxプロダクト事業、DTxプラットフォーム事業の内訳は開示していただけますか?
上野:セグメント別の業績予想については開示していません。
質問者:傾向だけでもけっこうですが、「SUSMED SourceDataSync」も含めて複数案件が走っているため、DTxプラットフォーム事業は増収となるという理解でよろしいでしょうか?
上野:細かい数字については開示できませんが、追加開発等を行ってきているため、DTxプラットフォーム事業についても事業収益を伸ばしていく方向です。
質問者:どちらのセグメントも増収の計画という理解でよろしいでしょうか?
上野:おっしゃるとおりです。
質疑応答:保険適用希望書提出後の認可までの期間について
質問者:中央社会保険医療協議会の状況を考えると、収載時期は2月、5月、8月、11月(注:2024年2月の厚生労働省保険局医療課の事務連絡によれば、正しくは医療機器については毎年3月、6月、9月及び12月が保険適用時期の基準となります)のため、年度内に収載されるには11月までに保険適用希望書を提出しないと収載の可能性は低いように思います。
御社が保険適用希望書を出してから3ヶ月で認可される可能性はあるのか、6ヶ月くらいを見ておいたほうがいいのか、どれくらいのスパンを考えておけばよいでしょうか?
上野:平均的な期間などについては厚生労働省などに出ているものもありますが、私どもではコントロールできないため、期間について私どもからお伝えする立場ではないというのが実際のところです。
質疑応答:保険適用希望書の再提出に向けた課題について
質問者:今後、御社が保険適用希望書を再提出し、その後の収載のところなどをコントロールできないことは理解しています。
現状、さらなるハードルは見つかっていないのでしょうか? 足元でデータを少し取り直したり、今までのデータについてレトロスペクティブ的な解析を行う必要はないという理解でよろしいでしょうか?
上野:おっしゃるとおりです。先ほどのご質問にもあったとおり、今まで規制当局の方々とコミュニケーションしてきた中で、保険収載の障害となるような事項の発生は認識していません。また、従前お伝えしているように、追加的な前向き試験を行う計画もありません。
質問者:そのような意味だと、素人考えではもう再提出してもいいのではと思ってしまいます。そこは省庁関係が承認しないと出せないものなのでしょうか?
上野:おっしゃるとおりです。手戻りをなくすために調整等をきちんと行い、必要な手続きについては省庁と相談した上で進めるかたちになると思います。
質問者:ただし、再提出の時期については現時点では非開示ということでしょうか?
上野:おっしゃるとおりです。
質疑応答:パイプラインの開発進捗について

質問者:パイプラインについて教えてください。スライド9ページと10ページに開発パイプライン、19ページに重点施策としてパイプラインの開発進捗を示しています。
例えば、19ページでは「SMD402」は「次試験の開始」と記載があります。

9ページのパイプライン表では探索的試験が終わり、次は検証的試験に進む段階だと思いますが、そのように捉えてよいでしょうか? 探索的試験をもう1本はさむのか、それとも最終試験になるのかではかなり意味合いが異なってくるため、解説をお願いします。
上野:おっしゃるとおり、「SMD401」「SMD402」「SMD201」については探索的試験が完了しています。一般的に次は検証的試験となりますが、この間に規制当局と試験プロトコルについて合意するかたちになります。規制当局との相談の中で、次にどのような試験を行うかが変わる可能性もあるということです。
私どもとしては極力コンパクトに行っていきたいと考えていますが、実施者側の判断として、場合によっては間に探索的試験をもう一度はさんだほうが時間軸は長くなるものの金銭的に効率的な場合もあるため、規制当局とのプロトコルに関する協議次第だと認識しています。そちらも含めて、現段階で準備している状況です。
質問者:「SMD402」などは今期の重点施策に「次試験の開始」とありますが、検証的試験の位置づけになるか、探索的試験がもう1本となるかはまだ決まっておらず、当局との相談次第ということでしょうか?
上野:おっしゃるとおりです。当局との相談がまず一義的にはあります。さらにその当局との相談後の合意をもとに、弊社としてどのように実施するのが適切かを別途判断するかたちだと認識しています。
関連銘柄
| 銘柄 | 株価 | 前日比 |
|---|---|---|
|
4263
|
1,088.0
(03/02)
|
-27.0
(-2.42%)
|
関連銘柄の最新ニュース
-
鼓動高まる「再生医療」関連株、薬事承認接近で株高新局面へ突入<株探... 03/02 19:30
-
前日に動いた銘柄 part2ユニチカ、マツモト、JMACSなど 03/02 07:32
-
前日に動いた銘柄 part2ユニチカ、マツモト、JMACSなど 02/28 07:32
-
東証グロース(大引け)=値上がり優勢、コーディア、WelbyがS高 02/27 15:33
-
東証グロース(前引け)=値上がり優勢、コーディアが一時S高 02/27 11:33
新着ニュース
新着ニュース一覧-
今日 00:11
-
今日 00:00
-
今日 00:00
-
03/02 23:55

